微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 某化学实验小组的同学为了探究SO2和氯水的漂白性,设计如下实验装置。
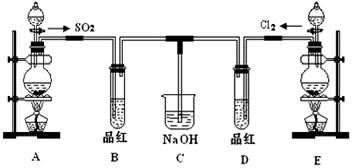
(1)C装置的作用:______________________________。
(2)实验室用装置E制备Cl2,化学反应方程式为:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O。该反应中的还原剂是____________(填化学式)。
MnCl2+Cl2↑+2H2O。该反应中的还原剂是____________(填化学式)。
(3)①反应开始一段时间后,观察到B、D两个试管中的品红溶液出现的现象是:
B_________________________, D________________________。
②停止通气后,再给B、D两个试管分别加热,两个试管中的现象分别为
B_________________________, D________________________。
(4)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后漂白性肯定会增强。他们将制得的SO2和Cl2按1:1同时通入到品红溶液中,结果发现品红溶液未退色。请你分析产生该现象的原因_____________________________来源:www.91exam.org(用化学方程式表示)。
参考答案:(1)尾气处理,吸收SO2和Cl2防止污染环境(2分)
本题解析:
试题分析:(1)C装置的作用是除去B中剩余的SO2和D项剩余的Cl2,故C的作用是尾气处理,吸收SO2和Cl2防止污染环境。
(2)MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O ?HCl作为还原剂,失去电子,发生氧化反应
MnCl2+Cl2↑+2H2O ?HCl作为还原剂,失去电子,发生氧化反应
(3)SO2和 Cl2都能使品红褪色 ,加热后B中褪色的品红
本题难度:一般
2、计算题 实验室迅速制备少量氯气可利用如下所示的反应
2KMnO4?+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O ; 当参加反应的氧化剂的物质的量是1mol时,回答下列问题:
(1)被氧化的还原剂的物质的量是多少?
(2)产生标准状况下的氯气的体积多少升?
参考答案:(1)5mol??(2)56L
本题解析:略
本题难度:一般
3、选择题 下列关于卤素的叙述中正确的是(???)
①卤素的钾盐中,最易被氧化的氟化钾;②溴中溶有少量氯气,可以用加入溴化钠再用汽油萃取的方法提纯;③溴化银具有感光性,碘化银不具感光性;④某溶液与淀粉碘化钾溶液反应出现蓝色,则证明该溶液是氯水或溴水;⑤氟气跟氯化钠水溶液反应,一定有HF和O2生成;⑥氯气跟水反应时,水既不是氧化剂也不是还原剂。
A.①③⑤
B.②④⑥
C.②⑤⑥
D.①③④
参考答案:C
本题解析:
试题分析:①卤素的钾盐中,最易被氧化的碘化钾,①错误;②溴中溶有少量氯气,可以用加入溴化钠再用汽油萃取的方法提纯,正确;③氯化银,溴化银和碘化银都具有感光性,③错误;④只能证明该溶液有氧化性,能与碘离子反应,不能证明是氯水或溴水,也可能是双氧水或硝酸溶液,④错误;⑤氟气先和水反应,所以得到的是HF和O2生成,⑤正确;⑥氯气跟水反应时,水既不是氧化剂也不是还原剂,正确。故选C.②⑤⑥
点评:本题考查卤族元素的化学性质,应注意有氧化性的水溶液不一定是氯水或溴水。
本题难度:简单
4、选择题 含有a mol FeBr2的溶液中,通入xmol Cl2。下列各项为通Cl2过程中,溶液内发生反应的离子方程式,其中不正确的是[???? ]
A.x=0.4a,2Fe2++Cl2=2Fe3++2Cl-
B.x=0.6a,2Br-+ Cl2=Br2+2Cl-
C.x=a,2Fe2++2Br-+2Cl2=Br2+2Fe3++4Cl-
D.x=1.5a,2Fe2++4Br-+3Cl2=2Br2+2Fe3++6Cl-
参考答案:B
本题解析:
本题难度:一般
5、选择题 有五瓶溶液分别是①10mL0.60mol・L-1NaOH水溶液②20mL0.5mol・L-1H2SO4水溶液③30mL0.40mol・L-1HCl水溶液④40mL0.30mol・L-1HCl水溶液⑤50mL0.20mol・L-1蔗糖水溶液。以上各瓶溶液所含离子、分子总数大小顺序是……( )
A.①>②>③>④>⑤
B.②>①>③>④>⑤
C.②>③>④>①>⑤
D.⑤>④>③>②>①
参考答案:A
本题解析:本题所问是溶液中的离子、分子总数,应包括溶质、溶剂以及由它们相互作用形成的离子。五瓶溶液溶质的浓度比较小,故主要取决于溶剂的量、,而溶液体积分别为10、20、30、40、50mL,依次增大。
本题难度:简单