微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 以下是依据一定的分类标准,对某些物质与水反应的情况进行分类的分类图。请根据你所学的知识,按要求填空:
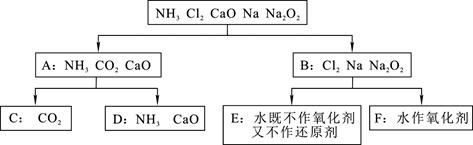
(1)上述物质的分类方法是?????????????????;
(2)根据物质与水反应的情况,分成A、B组的分类依据是????????(选择字母填空,下同),由A组分成C、D组的依据是?????????(填字母)。
a.与水反应后溶液的酸碱性?? b.与水反应的剧烈程度?? c.是否发生氧化还原反应
(3)F组的物质是???????????(填化学式)。
(4)A组中的酸性氧化物与B组中的某物质反应可用作呼吸面具或潜水艇中氧气的来源,其反应方程式为?????????????????????????????????????????????????????????。
参考答案:(6分)(1)树状分类法(1分);?(2)c(1分);a(1
本题解析:
试题分析:(1)根据示意图的结构特点可知,上述物质的分类方法是树状分类法。
(2)由于氨气、CO2和氧化钙在和水的反应都不是氧化还原反应,而氯气、钠和过氧化钠与水的反应是氧化还原反应,据此标准可以分类,答案选c。氨气和氧化钙溶于水,溶液显碱性,CO2溶于水显酸性,答案选a。
(3)钠和反应中,钠是还原剂,水是氧化剂,即F是钠。氯气、过氧化钠和水的反应中,水既不是氧化剂,也不是还原剂。
(4)过氧化钠和CO2反应生成氧气和过氧化钠,反应的化学方程式是2Na2O2 + 2CO2=2N
本题难度:一般
2、选择题 .将SO2气体与足量Fe2(SO4)3溶液完全反应后,再加入K2Cr2O7溶液,发生如下两个化学反应:SO2+2Fe3++2H2O===SO42-+4H++2Fe2+,Cr2O72-+6Fe2++14H+===2Cr3++6Fe3++7H2O。下列说法正确的是(???)
A.还原性:Cr3+>Fe2+>SO2
B.氧化性:Cr2O72->Fe3+>SO2
C.Cr2O72-不能将SO2氧化
D.两个反应中Fe2(SO4)3均作还原剂
参考答案:B
本题解析:根据在同一氧化还原反应氧化剂的氧化性大于氧化产物的氧化性;还原剂的还原性大于还原产物的还原性。故答案B正确。A、还原性SO2>Fe2+> Cr3+;C、重铬酸根具有强氧化性,可以氧化二氧化硫;D、第一反应中三价铁离子做氧化剂。
本题难度:简单
3、选择题 3.2 g Cu与30 mL 3 mol・L-1HNO3溶液充分反应,还原产物有NO2和NO,若反应后溶液中H+为a mol,则此时溶液中所含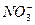 为(???)
为(???)
A.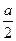 mol
mol
B.2a mol
C.0.1a mol
D.(a+0.1) mol
参考答案:D
本题解析:溶液中某元素的原子个数守恒,溶液中电荷守恒(即溶液显电中性)。根据题意,HNO3有剩余,则Cu反应完全。可据电荷守恒:n( )=2n(Cu2+)+n(H+)=2×
)=2n(Cu2+)+n(H+)=2×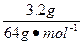 本题难度:简单
本题难度:简单
4、选择题 火药的爆炸反应为:2KNO3+S+3C====K2S+N2↑+3CO2↑,其中被还原的元素是
A.N
B.N和S
C.N和C
D.C
参考答案:B
本题解析:物质所含元素化合价降低被还原,所以根据化合价的变化可知,N和S的化合价降低,因此是还原剂。C的化合价升高,被氧化,答案选B。
本题难度:简单
5、填空题 部分弱酸的电离平衡常数如下表: