微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列关于能源的说法不正确的是
A.煤的干馏是物理变化,煤的气化和液化是化学变化
B.煤油可由石油分馏获得,可用作燃料和保存少量金属钠
C.沼气(主要成分是CH4)是可再生能源
D.太阳能、氢能、风能、地热能、生物质能都是新能源
参考答案:A
本题解析:
试题分析:A、煤的干馏是化学变化,故A错误;B、石油的分馏可得到汽油、煤油、柴油等产品,可用作燃料和保存少量金属钠,故B正确;C、沼气是有机物质在厌氧条件下,经过微生物的发酵作用而生成的一种混合气体,是可再生能源,故C正确;D、指刚开始开发利用或正在积极研究、有待推广的能源,如太阳能、氢能、地热能、风能、海洋能、生物质能和核聚变能等,故D正确。
考点:本题考查化学与能源。
本题难度:简单
2、计算题 (6分)常温下,将0.05mol/L盐酸溶液和未知浓度的NaOH溶液以1:2的体积比混合,所得溶液的pH=12。用上述NaOH溶液13 ml和pH=3的某一元弱酸HA溶液20ml恰好完全反应生成NaA。试求:
(1)NaOH溶液的物质的量浓度
(2)此一元弱酸的物质的量浓度
(3)求此条件下该一元弱酸的电离平衡常数
参考答案:(6分)(1)c(NaOH)=0.04mol/L?? (2)
本题解析:(1)两溶液混合后呈碱性,说明碱过量,设两溶液的体积分别为:V、2V
则: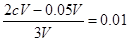 ,得c(NaOH)=0.04mol/L
,得c(NaOH)=0.04mol/L
(2)NaOH~HA,即:0.04×13=c(HA)×20,推出:c(HA)=0.026mol/L
(3)代入电离平衡常数公式:
K= 本题难度:一般
本题难度:一般
3、选择题 100 g碳燃烧所得气体中,CO占1/3 体积,CO2占 2/3 体积,且C(s)+ 1/2 O2(g)====CO(g) ΔH=-110.35 kJ・mol-1,CO(g)+ 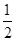 O2(g)====CO2(g) ΔH=-282.57 kJ・mol-1。与这些碳完全燃烧相比较,损失的热量是( )
O2(g)====CO2(g) ΔH=-282.57 kJ・mol-1。与这些碳完全燃烧相比较,损失的热量是( )
A.392.92 kJ
B.2 489.44 kJ
C.784.92 kJ
D.3 274.3 kJ
参考答案:C
本题解析:
试题分析:1mol碳完全燃烧生成二氧化碳气体放出的热量是110.35+282.57=392.92kJ,不完全燃烧时,损失的是生成的CO时少放出的热量,100g碳的物质的量是100/12=25/3mol,CO占1/3,说明有1/3×25/3=25/9mol的碳未完全燃烧,1mol碳不完全燃烧少放出的热量是282.57kJ,则25/9mol的碳不完全燃烧少放出的热量是25/9×282.57=784.92kJ,所以答案选C。
考点:考查化学反应热效应的计算
本题难度:一般
4、选择题 某温度下向20mL 0.1 mol・L-1 CH3COOH溶液中逐滴加入0.1 mol・L-1 NaOH溶液,混合液的pH随NaOH溶液的体积(V)的变化关系如图(忽略温度变化)。下列说法中正确的是(??)
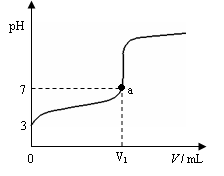
A.该温度下醋酸的电离平衡常数约为1×10-5mol・L-1
B.图中V1 > 20mL,且a点对应的溶液中:
c (Na+)+ c (H+) = c (OH-)+ c (CH3COO-)
C.图中V1 < 20mL,且a点对应的溶液中:
c (CH3COOH) + c (CH3COO-)<c (Na+)
D.当加入Na OH溶液的体积为20mL时,溶液中:
c (CH3COOH) + c (H+) > c (OH-)
参考答案:A
本题解析:A正确,醋酸的电离常数 ;B错,若V1 = 20mL,则CH3COOH与NaOH恰好完全反应生成CH3COONa,溶液显碱性,因溶液此时显中性,所以,V1 < 20mL;C错,由于解得,V1 < 20mL,所以此时溶液中的溶质为CH3COONa和CH3COOH,即可得c (CH3COOH) + c (CH3COO
;B错,若V1 = 20mL,则CH3COOH与NaOH恰好完全反应生成CH3COONa,溶液显碱性,因溶液此时显中性,所以,V1 < 20mL;C错,由于解得,V1 < 20mL,所以此时溶液中的溶质为CH3COONa和CH3COOH,即可得c (CH3COOH) + c (CH3COO
本题难度:一般
5、选择题 草酸是二元中强酸,草酸氢钠溶液显酸性。常温下,向10 mL 0.01 mol/L NaHC2O4溶液中滴加0.01 mol/L NaOH溶液,随着NaOH溶液体积的增加,溶液中离子浓度关系正确的是
A.V(NaOH)="=" 0时,c(H+,W)="=" 1 × 10-2 mol/L
B.V(NaOH)< 10 mL时,不可能存在c(Na+)="=" 2 c(C2O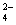 )+ c(HC2O
)+ c(HC2O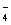 )
)
C.V(NaOH)="=" 10 mL时,c(H+,W)="=" 1 × 10-7mol/L
D.V(NaOH)> 10 mL时,c(Na+)> c(C2O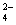 )>c(HC2O
)>c(HC2O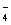 )
)
参考答案:D
本题解析:
试题分析:草酸是二元中强酸,草酸氢钠溶液显酸性,这说明HC2O4-的水解程度小于HC2O4-的电离程度,但电离是不彻底的,所以溶液中氢离子的浓度小于0.01mol/L,A不正确;当V(NaOH)="=" 10 mL时,二者恰好反应时生成草酸钠,水解溶液显碱性。根据电荷守恒可知c(H+)+c(Na+)=" 2" c(C2O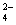 本题难度:简单
本题难度:简单