微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 下图所示是中学化学里常见纯净物A―L间的反应关系,其中A、H、E、F为单质且E、F为气体,B在常温下是无色液体,C是淡黄色固体,L是红褐色固体。
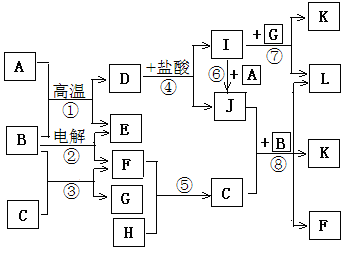
请根据图示判断并回答下列问题:
(1)单质A中所含元素在周期表中的位置是 ;
(2)反应③的化学方程式为 ;
(3)反应④的离子方程式为 ;
(4)反应⑧的离子方程式为 ;
(5)反应②发生过程中,当有3.01×1024个电子发生转移时,电解消耗物质B的质量为 g,同时阴极生成的气体的体积为 L(换算为标准状况下的体积)。
参考答案:(1)第四周期Ⅷ族(2分)
(2)2Na2O2+2H2
本题解析:
试题分析:本题突破点在与B在常温下是无色液体,故B为谁,C为淡黄色固体,能与水反应生成G溶液与F气体单质,故C为Na2O2,G为NaOH,F为O2;L为红褐色固体,为Fe(OH)3,由D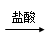 I溶液可知I为FeCl3,J为FeCl2,A为单质铁。从而可以推导出其他物质分别为:A为Fe,B为H2O,C为Na2O2,D为Fe3O4,E为H2,F为O2,G为NaOH,H为Na,I为FeCl3,J为FeCl2,K为NaCl。(1)单质A为金属Fe,在元素周期表的位置为第四周期Ⅷ族。(2)反应③为水与过氧化钠的反应,离子反应方程式为2Na2O2+2H2O=4NaOH+O2↑(3)反应④的反应为四氧化三铁和盐酸的反应,故离子反应方程式为Fe3O4+8H+=Fe2++2Fe3++4H2O。(4)反应⑧为水与过氧化钠和氯化亚铁的反应,离子反应方程式为4Na2O2+4Fe2++6H2O=8Na++4Fe(OH)3↓+ O2↑(5)反应②为电解水的反应,反应方程式为2H2O
I溶液可知I为FeCl3,J为FeCl2,A为单质铁。从而可以推导出其他物质分别为:A为Fe,B为H2O,C为Na2O2,D为Fe3O4,E为H2,F为O2,G为NaOH,H为Na,I为FeCl3,J为FeCl2,K为NaCl。(1)单质A为金属Fe,在元素周期表的位置为第四周期Ⅷ族。(2)反应③为水与过氧化钠的反应,离子反应方程式为2Na2O2+2H2O=4NaOH+O2↑(3)反应④的反应为四氧化三铁和盐酸的反应,故离子反应方程式为Fe3O4+8H+=Fe2++2Fe3++4H2O。(4)反应⑧为水与过氧化钠和氯化亚铁的反应,离子反应方程式为4Na2O2+4Fe2++6H2O=8Na++4Fe(OH)3↓+ O2↑(5)反应②为电解水的反应,反应方程式为2H2O 2H2↑+O2↑,当有3.01×1024个电子发生转移时有2.5mol水被电解,即有45g水被消耗。阴极生成的气体为氢气,且产生的氢气与电解水的物质的量相等,都为2.5mol。故转化成体积为22.4L/mol×2.5mol=56L。
2H2↑+O2↑,当有3.01×1024个电子发生转移时有2.5mol水被电解,即有45g水被消耗。阴极生成的气体为氢气,且产生的氢气与电解水的物质的量相等,都为2.5mol。故转化成体积为22.4L/mol×2.5mol=56L。
考点:无机推断,离子反应方程式书写
本题难度:困难
2、选择题 下列离子方程式书写正确的是
A.向NaHSO4溶液中滴入Ba(OH)2溶液至中性:H++SO42-+Ba2++OH- = BaSO4↓+H2O
B.NaClO溶液与FeCl2溶液混合:Fe2+ + 2ClO- + 2H2O = Fe(OH)2↓ + 2HClO
C.NH4HSO3溶液与足量NaOH溶液反应:NH4+ + OH-= NH3↑ + H2O
D.将1mol/LNaAlO2溶液和1.5mol/L的HCl溶液等体积均匀混合:6AlO2-+9H++3H2O=5Al(OH)3↓+Al3+
参考答案:D
本题解析:
试题分析:A不正确,应该是2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O;B不正确,次氯酸钠具有强氧化性,能把氯化亚铁氧化生成铁离子;C不正确,反应中还有亚硫酸钠生成,所以正确的答案选D。
考点:考查离子方程式的正误判断
点评:该题是高考中的高频题,属于中等难度的试题,旨在对学生能力的培养和训练。该题需要明确判断离子方程式正确与否的方法一般,即(1) 检查反应能否发生。(2)检查反应物、生成物是否正确。(3)检查各物质拆分是否正确。(4)检查是否符合守恒关系(如:质量守恒和电荷守恒等)。(5)检查是否符合原化学方程式,然后灵活运用即可。该题有助于培养学生分析问题、解决问题的能力。
本题难度:困难
3、选择题 下列化学反应的离子方程式书写不正确的是
A.碳酸钙与盐酸的反应:CaCO3 +2H+ =Ca2++ CO2↑+ H2O
B.等物质的量的MgCl2、Ba(OH)2和HCl溶液混合: Mg2++2OH-=Mg(OH)2↓
C.氧化铜与稀H2SO4反应:CuO+2H+ =Cu2+ + H2O
D.金属钠跟水反应: 2Na+2H2O=2Na++ 2OH- +H2↑
参考答案:B
本题解析:
试题分析:等物质的量的MgCl2、Ba(OH)2和HCl溶液混合,离子方程式为H++ OH-= H2O,选B。
考点:考查离子方程式的正误判断。
本题难度:一般
4、选择题 类推思维是化学解题中常用的一种思维方法,下列有关离子方程式的类推正确的是
| 已知
| 类推
|
A
| 将Fe加入CuSO4溶液中:Fe+Cu2+=Cu+Fe2+
| 将Na加入到CuSO4溶液中:2Na+Cu2+=Cu+2Na+
|
B
| 向Ca(ClO)2溶液中通入少量CO2
CO2+H2O+Ca2++2ClO-=CaCO3↓+2HClO
| 向Ca(ClO)2溶液中通入少量SO2
SO2+H2O+Ca2++2ClO-=CaSO3↓+2HClO
|
C
| 惰性电极电解氯化钠溶液
2Cl-+2H2O 2OH-+H2↑+Cl2↑ 2OH-+H2↑+Cl2↑
| 惰性电极电解MgBr2溶液
2Br-+2H2O 2OH-+H2↑+Br2 2OH-+H2↑+Br2
|
D
| 稀盐酸与NaOH溶液反应至中性
H++OH-=H2O
| 稀硝酸与Ba(OH)2溶液反应至中性
H++OH-=H2O
参考答案:D
本题解析:
试题分析:A、铁排在金属铜的前面,金属铁可以将金属铜从其盐中置换出来,但是活泼金属钠和盐溶液的反应是先与水反应,不会置换出其中的金属,故A错误;B、同时和亚硫酸的酸性均强于次氯酸,但SO2具有还原性,次氯酸钙含有氧化性,二者混合发生氧化还原反应,B错误;C、惰性电极电解溴化镁溶液生成氢氧化镁沉淀、氢气和溴,C错误;D、盐酸与氢氧化钠、稀硝酸与氢氧化钡反应均可用H++OH-=H2O不是,D正确,答案选D。
考点:考查离子方程式书写知识
本题难度:一般
5、填空题 现有下列十种物质:①液态HCl ②NaHCO3 ③NaCl溶液 ④CO2 ⑤蔗糖晶体 ⑥Ba(OH)2 ⑦红褐色的氢氧化铁胶体 ⑧NH3・H2O ⑨空气 ⑩Al2(SO4)3
(1)上述十种物质中有两种物质在水溶液中可发生反应,离子方程式为:H++OH-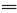 H2O,该反应的化学方程式为 。 H2O,该反应的化学方程式为 。
(2)⑩在水中的电离方程式为 ,
(3)胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉,易吐酸水,服用适量的小苏打(NaHCO3),能治疗胃酸过多,请写出其反应的离子方程式: ;如果病人同时患胃溃疡,为防胃壁穿孔,不能服用小苏打,此时最好用含Al(OH)3的胃药(如胃舒平),它与胃酸反应的离子方程式:
(4)向Ba(OH)2溶液中逐滴加入稀硫酸,请完成下列问题:
①写出反应的离子方程式 。
参考答案:27、(1)Ba(OH)2+2HCl=BaCl2+2H2O;
本题解析:
本题难度:一般
|