12.0
(3)写出向沉淀物A中加入过量氢氧化钠溶液的离子方程式???????????????????。
(4)①某同学在实验室中用图1装置制取CO2气体并通入溶液Ⅱ中,结果没有沉淀产生,可能的原是??????????????;为了能产生沉淀,该同学对图1装置进行了改进,改进的方法为?????????。

②若将二氧化碳气体通入澄清石灰水中,石灰水变浑浊,混合体系中除存在电离平衡、水解平衡外,还存在溶解平衡,用方程式表示该溶解平衡关系???????????????????????????。
参考答案:(1) Fe3+ Al3+(2)Al(OH)3? Ca(OH
本题解析:
试题分析:榴石矿石中氧化钙、氧化铝、氧化铁与盐酸生成氯化钙、氯化铝、氯化铁,二氧化硅不反应。溶液I中控制pH=9~10,使Fe3+、Al3+完全沉淀,Ca2+不沉淀,若氢氧化钠过量,则氢氧化铝溶解,Ca2+也形成沉淀。沉淀物A为氢氧化铝和氢氧化铁的混合物,加入过量氢氧化钠溶液,氢氧化铝溶解生成偏铝酸钠,氢氧化铁不溶,向偏铝酸钠、氢氧化钠混合溶液中通入过量二氧化碳气体生成氢氧化铝和碳酸氢钠。将大理石与盐酸产生的二氧化碳气体通入偏铝酸钠、氢氧化钠混合溶液中无沉淀产生可能原因是二氧化碳气体中含有大量氯化
本题难度:一般
2、选择题 (15分)下图是无机物A~M在一定条件下的转化关系(部分产物及反应条件未列出)。其中,I是第三周期原子半径最小的金属元素组成的单质,D是一种红棕色固体粉末,G为单质,K是一种红棕色气体,A、B相对分子质量相差16,J、C都是常见的强酸。

请填写下列空白:????????????????????????????????????????????????
(1)写出下列物质的化学式B??????????E????????????。
(2)反应⑦的化学方程式为????????????????????????。反应⑦属于???????????。
A.吸热反应???? B.放热反应???? C.置换反应????? D.氧化还原反应??????????????????????????????????????????
(3)反应⑩的离子方程式为?????????????????????????????????????????????????????。
(4)将化合物D与KNO3、KOH混合,在高温条件下可制得一种“绿色”环保高效净水剂K2GO4(G显+6价),同时还生成KNO2和H2O。该反应的化学方程式是:???????????????????????????????。?
(5)反应①中生成的A、D物质的量之比为4:1,已知甲矿石的主要成分是由两种元素组成的化合物,则该化合物的化学式为????????????????。
参考答案:(1)B? SO3 ?E? Fe(OH)3; (2)?Fe2
本题解析:
试题分析:(1)甲矿石是FeS2,矿石煅烧得到A:SO2和D:Fe2O3;SO2与O2发生反应得到B:SO3,SO3与水作用得到C:硫酸;I是Al,Al与Fe2O3发生铝热反应:Fe2O3+ 2Al Al2O3+2Fe,得到的G的Fe;H是Al2O3。E是Fe(OH)3;F是Fe2(SO4)3和Fe(NO Al2O3+2Fe,得到的G的Fe;H是Al2O3。E是Fe(OH)3;F是Fe2(SO4)3和Fe(NO
本题难度:一般
3、推断题 有X、Y、Z三种元素,已知
①X、Y、Z的单质在常温下均为气体??
②X单质可在Z单质中燃烧,生成XZ,火焰为苍白色??
③XZ极易溶于水,电离出X+和Z-,其水溶液可使蓝色石蕊试纸变红??
④每2个X2分子可与1个Y2分子化合生成2个X2Y分子,X2Y在常温下为液体??
⑤Z单质溶于X2Y中,所得溶液具有漂白作用。
(1)推断X、Y、Z三种元素的名称为X.?__________,Y.?_________,Z.?_________。
(2)化合物的化学式XZ_______________,X2Y_________________。
(3)五个过程中涉及的化学反应的方程式为_____________________、______________________、______________________。
参考答案:(1)氢;氧;氯??
(2)HCl;H2O
(3
本题解析:
本题难度:一般
4、简答题 下列转化关系图中,A、B、C、D、E常温下为气体,B、E、F、K为单质,其中F为黑色固体;C、D均能使澄清的石灰水变混浊,D、E均能使品红溶液褪色;I是一种红棕色固体氧化物.请回答下列问题:
(1)E的电子式为______.
(2)反应③的离子方程式为______.
(3)F与G的溶液反应的化学方程式为______.
(4)检验溶液L中金属阳离子的方法是______.
(5)气体A的密度为相同状况下氢气密度的30倍,且A中含3种组成元素,通过计算、推理,可确定A的分子式为______(此分子式中元素符号书写次序按从左往右元素原子序数“大小中”顺序排列);A分子中各原子均达8电子稳定结构,则其结构式为______.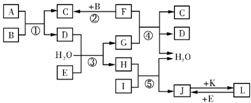
参考答案:C、D均能使澄清的石灰水变混浊,能使澄清石灰水变浑浊的气体有
本题解析:
本题难度:一般
5、推断题 已知X溶液有如图所示转化关系:

(1)根据上述转化关系,写出下列物质的化学式:X________、Y________、Z?_______、试剂甲_______,试剂乙_______?。
(2)写出上述各步反应①~④的离子方程式:
①______________;②______________;③_____________;④_______________?。
参考答案:(1)X:MgSO4;Y:Mg(OH)2;Z:MgCl2;试
本题解析:
本题难度:一般
|