23.5��
��֪��Q=cm(t2 -t1)����Ӧ����Һ�ı�����cΪ4.18J����-1�� g-1�������ʵ��ܶȾ�Ϊ1g��cm-3��
����ʵ����д��NaOH��Һ��HCl��Һ��Ӧ���Ȼ�ѧ����ʽ����Hֵ��ȷ��С�����2λ����
???????????????????????????????????????????????????????????????????????��4������KOH����NaOH���Բⶨ���??????����С����ޡ���Ӱ�졣
�ο��𰸣���13�֣�
��1����Ͳ??�¶ȼƣ�4�֣�
��2��
���������
���������ʵ�����ϱ����ձ�����С�����ձ�������ĭ���ϡ���ĭ���ϰ塢��ͷ�ιܡ����β����������0.5mol�� L-1���ᡢ0.55mol�� L-1NaOH��Һ����ȱ�ٵ�ʵ�鲣����Ʒ����Ͳ??�¶ȼƣ�ʵ���в����û���ͭ˿��������滷�β������������Ϊͭ˿���������ã�����к��ȵļ������Ӱ�죻��֪��Q=cm(t2 -t1)����Ӧ����Һ�ı�����cΪ4.18J����-1�� g-1�������ʵ��ܶȾ�Ϊ1g��cm-3��NaOH��Һ��HCl��Һ��Ӧ���Ȼ�ѧ����ʽ��NaOH(aq)+HCl(aq)=NaCl(aq)+
�����Ѷȣ�һ��
2��ѡ���� ����˵�����ʾ��ȷ���ǣ�������
A�������ʵ������������������ֱ���ȫȼ�գ����߷ų�������
B���ɵ���Aת��Ϊ����B����H=+119kJ/mol����֪����B�ȵ���A�ȶ�
C��ϡ��Һ�У�H+��aq��+OH-��aq���TH2O��l����H=-57.3kJ/mol��������0.5mol��Ũ�����뺬1molNaOH����Һ��ϣ��ų�����������57.3kJ
D����101kPaʱ��2gH2��ȫȼ������Һ̬ˮ���ų�285.8kJ��������H2ȼ���ȵ��Ȼ�ѧ����ʽ�ɱ�ʾΪ��2H2��g��+O2��g���T2H2O��l��H=-571.6kJ/mol
�ο��𰸣�A���������仯Ϊ�����Ϊ���ȹ��̣�������������������������
���������
�����Ѷȣ�һ��
3��ѡ���� ��֪�Ȼ�ѧ����ʽC2H2��g��+5/2O2��g��=2CO2��g��+H2O��g������H=-1256kJ/mol������˵����ȷ����
A����Ȳ��ȼ����Ϊ1256kJ/mol
B����ת��10mol���ӣ�������2.5molO2
C��������2molҺ̬ˮ�����H=-2512kJ/mol
D�����γ�4mol̼�����õ��Ӷԣ���ų�������Ϊ2512kJ
�ο��𰸣�B
���������
��ȷ�𰸣�B
A������ȷ��ˮ����Һ̬��B��ȷ��C������ȷ�������������̬ˮ��D������ȷ��1molCO2�γ�4mol���õ��Ӷԣ��ų�������Ϊ628kJ
�����Ѷȣ�һ��
4��ѡ���� ��״̬�£���̬���ӶϿ�l mol��ѧ�����ʱ��Ϊ���ʡ���֪H-H��H-O��O-O���ļ��ʦ�H�ֱ�Ϊ436 kJ/mol��463 kJ/mol��495kJ/mol�������Ȼ�ѧ����ʽ��ȷ����
A��H2O (g)= H2(g)+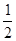 O2(g); ��H=" -485" kJ/mol O2(g); ��H=" -485" kJ/mol
B��H2O (g)=H2(g)+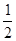 O2(g); ��H="=+485" kJ/mol O2(g); ��H="=+485" kJ/mol
C��2H2(g)+ O2 (g)= 2H2O(g) ��H =" +485" kJ/mol
D��2H2(g)+ O 2(g)=2H2O(g) ��H =" -485" kJ/mol
�ο��𰸣�D
���������
��������� 1mol����̬ˮ�ֽ����1mol��������1/2mol�������������仯�ǣ�2��463 kJ-436��1/2��495="242." 5.����Ȼ�ѧ����ʽΪH2O (g)= H2(g)+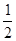 O2(g);? ��H=" +242." 5kJ/mol��A.B����������2mol����̬ˮ�ֽ����2mol������ O2(g);? ��H=" +242." 5kJ/mol��A.B����������2mol����̬ˮ�ֽ����2mol������
�����Ѷȣ�һ��
5��ѡ���� ��֪ǿ����ǿ����ϡ��Һ�ﷴӦ���к��ȿɱ�ʾΪ��
H��(aq)��OH��(aq)===H2O(l)����H����57.3 kJ/mol,�����з�Ӧ��
CH3COOH(aq)��NaOH(aq)===CH3COONa(aq)��H2O(l)����H����Q1 kJ/mol[
H2SO4(Ũ)��NaOH(aq)===Na2SO4(aq)��H2O(l)����H����Q2 kJ/mol
HNO3(aq)��NaOH(aq)===NaNO3(aq)��H2O(l)?? ��H����Q3 kJ/mol
������Ӧ������Һ�н��У�������Q1��Q2��Q3�Ĺ�ϵ��ȷ����
A��Q2>Q3>Q1
B��Q2>Q1>Q3
C��Q1��Q2��Q3
D��Q2��Q3>Q1
�ο��𰸣�A
���������CH3COOH(aq)��NaOH(aq)===CH3COONa(aq)��H2O(l)��Ϊ������ǿ�Ӧ����������H+ʱҪ�������������Ը÷�Ӧ�ų�������57.3 kJ�٣�H2SO4(Ũ)��NaOH(aq)===Na2SO4(aq)��H2O(l)����Ӧ�У�Ũ����ϡ�ͻ��ȣ������������ͷŵ���࣬������57.3 kJ��HNO3(aq)��NaOH(aq)===NaNO3(aq)��H2O(l)����ǿ����ǿ�Ӧ���ͷŵ�����Ϊ57.3 kJ��
���ԣ����ϵΪ��Q2>Q3>
�����Ѷȣ�һ��
|