微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 化学实验中常将溶液或试剂进行酸化,下列酸化处理的措施正确的是?
A.定性检验SO,将BaCl2溶液用HNO3酸化
B.为提高高锰酸钾 溶液的氧化能力,用盐酸将高锰酸钾溶液酸化
溶液的氧化能力,用盐酸将高锰酸钾溶液酸化
C.检验溶液中是否含有Fe2+时,用硝酸酸化
D.检验溶液中是否含有SO时,在无其他阳离子干扰的条件下,先用盐酸酸化,所得溶液再加BaCl2溶液
参考答案:D
本题解析:略
本题难度:一般
2、选择题
A.NaCl溶液、MgCl2溶液、KNO3溶液、Al2(SO4)3溶液
B.苯、苯酚溶液、己烯和乙醇
C.Na2SO4溶液、Na2SO3溶液、Na2CO3溶液、NaAlO2溶液
D.NaCl溶液、NH4Cl溶液、(NH4)2SO4溶液、Na2SO4溶液
参考答案:A
本题解析:B项可用溴水鉴别,C项可用盐酸鉴别,D项可作Ba(OH)2鉴别,只有A项不行。
本题难度:一般
3、选择题 下列各项叙述中正确的是
A.2gH2所含原子数约为6.02×1023
B.H2SO4的摩尔质量是98g
C.11.2LO2的质量是16g
D.1mol水的质量是18g
参考答案:D
本题解析:分析:A、利用n=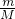 及N=n×NA来计算;
及N=n×NA来计算;
B、摩尔质量的单位为g/mol;
C、不知道状况,则无法利用体积计算物质的量;
D、利用m=n×M来计算质量.
解答:A、氢气的物质的量为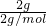 =1mol,原子数约为1×2×6.02×1023=2×6.02×1023,故A错误;
=1mol,原子数约为1×2×6.02×1023=2×6.02×1023,故A错误;
B、H2SO4的摩尔质量是98g/mol,故B错误;
C、不一定是在标准状况下,Vm不知,无法利用体积计算物质的量,故C错误;
D、水的质量为1mol×18g/mol=18g,故D正确;
故选D.
点评:本题考查物质的量的计算,明确物质的质量、体积与物质的量的关系即可解答,注意C项学生容易忽略是否在标准状况下而错选.
本题难度:简单
4、选择题 有一未知浓度的盐酸溶液25?mL,在加入0.5?mol・L-1?AgNO3溶液25??mL后,改加NaOH溶液,结果用去0.1?mol・L-1NaOH溶液25?mL,恰好完全中和,则盐酸的物质的量浓度为
A.0.2 mol・L-1
B.0.5 mol・L-1
C.0.1 mol・L-1
D.0.25 mol・L1
参考答案:C
本题解析:本题是利用元素守恒的原则进行的计算,AgNO3溶液不消耗H+。H+ + OH- == H2O由于盐酸和NaOH体积相同,所以浓度相同。
以后同学们在做这种类型的题时,一定要审准题,不要被题目中所设的陷阱所迷惑。
本题难度:困难
5、填空题 (1)鉴别KCl溶液和K2CO3的试剂是______,离子方程式为______.
(2)除去混入NaCl溶液中少量NaHCO3杂质的试剂是______,离子方程式为______.
(3)除去Na2CO3粉末中混入的NaHCO3杂质用______方法,化学方程式为______.
参考答案:(1)因KCl不能和盐酸反应,K2CO3能与盐酸反应生成氯化
本题解析:
本题难度:一般