��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� 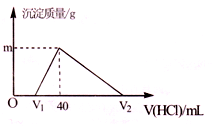 �����£���ag�����Ͻ��ĩ����һ����ˮ�У������ȫ���ܽ⣬�ռ���b?mL���壨��״������Ȼ������Һ�м���1mol/L�����ᣬ���ɳ�������������������������ϵ��ͼ��ʾ����V1=20mL�������й�ϵ��ȷ����
�����£���ag�����Ͻ��ĩ����һ����ˮ�У������ȫ���ܽ⣬�ռ���b?mL���壨��״������Ȼ������Һ�м���1mol/L�����ᣬ���ɳ�������������������������ϵ��ͼ��ʾ����V1=20mL�������й�ϵ��ȷ����
A.a=0.92
B.b=896
C.m=1.56
D.V2=100
�ο��𰸣�CD
��������� �����������Ͻ�����ˮ�У��Ͻ�ȫ���ܽ⣬����2Na+2H2O�T2NaOH+H2����2Al+2H2O+2NaOH�T2NaAlO2+3H2����
��ͼ���֪����������û���������������������ȷ�����ӦNaOH+HCl�TNaCl+H2O���ý���������20mL��
Ȼ������ӦNaAlO2+HCl+H2O�TNaCl+Al��OH��3����������������������40mLʱ���������ֵ����ʱ��Һ������ΪNaCl������Ԫ���غ��֪n��Na��=n��NaCl�����ý������������Ϊ40mL-20mL=20mL�����ݷ���ʽ����n[Al��OH��3]��������Ԫ���غ�n��Al��=n[Al��OH��3]��
�������ӦAl��OH��3��+3HCl�TAlCl3+3H2O�������������������ʵ�������ý���������������
A������m=nM����Na��Al�Ͻ��������
B������Na��Al�����ʵ�������������������������ٸ���V=nVm�������ɵ������������
C�������������������ʵ���������m=nM��������������������
D���ܽ������������ĵ����������40mL֮��ΪV2��ֵ��
��������Ͻ�����ˮ�У��Ͻ�ȫ���ܽ⣬����2Na+2H2O�T2NaOH+H2����2Al+2H2O+2NaOH�T2NaAlO2+3H2����
��ͼ���֪����������û���������������������ȷ�����ӦNaOH+HCl�TNaCl+H2O���ý���������20mL��
Ȼ������ӦNaAlO2+HCl+H2O�TNaCl+Al��OH��3����������������������40mLʱ���������ֵ����ʱ��Һ������ΪNaCl������Ԫ���غ��֪n��Na��=n��NaCl��=0.04L��1mol/L=0.04mol���ý������������Ϊ40mL-20mL=20mL�����ݷ���ʽ����n[Al��OH��3]=n��HCl��=0.02L��1mol/L=0.02mol��������Ԫ���غ�n��Al��=n[Al��OH��3]=0.02mol��
�������ӦAl��OH��3��+3HCl�TAlCl3+3H2O��������������ʵ���Ϊ0.02mol��3=0.06mol���ʸý����ĵ��������Ϊ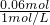 =0.06L=60mL��
=0.06L=60mL��
A��������������֪��Na��Al�Ͻ������Ϊ0.04mol��23g/mol+0.02mol��27g/mol=1.46g����A����
B���ɷ���ʽ��֪��0.04molNa��������Ϊ0.04mol�� =0.02mol��0.02molAl��������Ϊ0.02mol��
=0.02mol��0.02molAl��������Ϊ0.02mol�� =0.03mol�����������������ʵ���Ϊ0.02mol+0.03mol=0.05mol�������µ����Ϊ0.05mol��22.4L/mol=1.12L����B����
=0.03mol�����������������ʵ���Ϊ0.02mol+0.03mol=0.05mol�������µ����Ϊ0.05mol��22.4L/mol=1.12L����B����
C�������������֪�����ɳ���Ϊ0.02mol��������Ϊ0.02mol��78g/mol=1.56g����C��ȷ��
D�������������֪���ܽ���������������������Ϊ60mL����V2Ϊ40mL+60mL=100mL����D��ȷ��
��ѡCD��
���������⿼��������йؼ��㼰�ơ����Ļ�ѧ���ʵȣ���ȷ�����Ļ�ѧ��Ӧ����Ӧ��ͼ��Ķ�Ӧ��ϵ�ǽ����Ĺؼ���ע������Ԫ���غ�ķ���������ѶȽϴ�
�����Ѷȣ���
2��ѡ���� �����й����ʷ������ɵ�˵���У���ȷ��һ����
�ٷ������ѻ����ǻ�ѧ�仯
�����ᡢƯ�ۡ�ˮ�������ǻ����
��ֲ���͡�ֱ�����Ͷ�������ˮ��Ӧ
��������ʯ�ࡢ�����ᡢˮ���ǵ����
�ݾ���ϩ��������ϩ����ά�ض����ںϳɸ߷���
�����Ǻ���ѿ�ǵĻ�ѧʽ����C12H22O11�����ǻ�Ϊͬ���칹�壮
A.�ڢܢ�
B.�٢ۢ�
C.�٢ۢ�
D.�ڢݢ�
�ο��𰸣�A
����������������ٷ���������Һ��е��������������ķ������ڻ�����������ֻ��������ϵ�������ɣ���ֱ����������Ҫ�������������ܸ�����ˮ�л��ۻ�״̬���ܷ����Ļ���������������ʣ�����ά������Ȼ�߷��ӻ��������ʽ��ͬ�����ṹ��ͬ���л������ﻥΪͬ���칹�壮
��𣺢ٸ����ѻ��ǻ�ѧ�仯�����������������仯���ʢٴ���
����������HCl��ˮ��ɣ�Ư�۵���Ҫ�ɷ�Ϊ�Ȼ��ƺʹ�����ƣ�ˮ�����ǹ����Ƶ�ˮ��Һ�������ڻ����ʢ���ȷ��
��ֲ�����к��в����ͼ���������ˮ��Ӧ����ֱ����������Ҫ������������������ˮ��Ӧ���ʢ۴���
��������ʯ�ࡢ�����ᡢˮ���ǻ������ˮ�л��ۻ�״̬���ܵ��룬�����ڵ���ʣ��ʢ���ȷ��
�ݾ���ϩ��������ϩ�����üӾ۷�Ӧ���ɵĺϳɸ߷��ӣ�����ά������Ȼ�߷��ӻ�����ʢݴ���
�����Ǻ���ѿ�ǵķ���ʽ��ͬ�����ṹ��ͬ����ѿ�Ǿ��л�ԭ�ԣ������Dz����У�����Ϊͬ���칹�壬�ʢ���ȷ��
��ѡA��
���������⿼���˽϶�Ļ���֪ʶ��ע���˻�������Ŀ��飬ѧ��ֻҪ��Ϥ��������е�Ҫ�㣬ע��ƽʱ�Ļ��ۼ��ɽ��
�����Ѷȣ�����
3��ѡ���� ��Ȼ��������Ϊ����ɫ������ʡһЩ��������Ϊԭ�ϣ��ӹ�������һ��ѩ������ɫ�����ѩ��������������£��������ѷ��ڷ�յúܺõ����ϴ����ڣ�������һ��֧һ�ڹ������ڷ�����ƣ�����ʹ����ۻ���ȼ�գ��������ң�ѩ�����Ƴ��ˣ������ַ����Ƶõ�ѩ�����������ã����Ҷ�����Ҳ��Σ��������ѩ�����õ���
A.���������
B.���Ư����
C.SO2��������
D.SO2��Ư������
�ο��𰸣�D
��������������ɵ���ɫת��Ϊ��ɫ��˵���л�ɫ�ʱ�SO2Ư�ף�
�����Ѷȣ�����
4��ѡ���� ��ʹ0.1 mol/L NaHCO3��Һ��c(H��)��c(CO)��c(HCO)�����٣��䷽����
A.ͨ�������̼����
B.�����������ƹ���
C.ͨ���Ȼ�������
D.���뱥��ʯ��ˮ��Һ
�ο��𰸣�D
������������������A������CO2��H2O H2CO3
H2CO3 H����HCO��ʹc(HCO)����B�з�Ӧ��NaHCO3��NaOH��Na2CO3��H2O��c(CO)����C������HCl����ˮ�����H��������ʹc(H��)����D�з�Ӧ��NaHCO3��Ca(OH)2��CaCO3����H2O��NaOH����D����Ҫ��ѡD��
H����HCO��ʹc(HCO)����B�з�Ӧ��NaHCO3��NaOH��Na2CO3��H2O��c(CO)����C������HCl����ˮ�����H��������ʹc(H��)����D�з�Ӧ��NaHCO3��Ca(OH)2��CaCO3����H2O��NaOH����D����Ҫ��ѡD��
���㣺����̼�����ƵĻ�ѧ����
�����������Ǹ߿��еij������ͣ������е��Ѷȵ����⣬���������ǿ���������ض�ѧ�������Ŀ��顣����Ĺؼ���������ס̼�����ƵĻ�ѧ���ʣ�Ȼ��������ü��ɡ�
�����Ѷȣ�����
5��ѡ���� ��Ũ������ﳱʪ������������������
A.������
B.��ˮ��
C.��ˮ��
D.����
�ο��𰸣�C
���������������Ũ���������ˮ�ԣ��������������������������ʲ���������������Ӧ��
���Ũ���������ˮ�ԣ����������������������Ũ������ﳱʪ��������
��ѡC��
���������⿼���˳��������ʸ��������ɴ��⣬��������Ũ��������ʽ��У�
�����Ѷȣ�����