微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 (10分)为比较Fe3+和Cu2+对H2O2分解的催化效果甲乙两组同学分别设计了如图一、图二所示的实验。
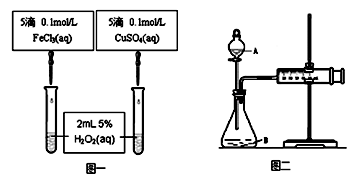
(1)图一可通过观察_____________________________ 现象来定性比较得出结论。有同学提出将CuSO4改为CuCl2更为合理,其理由是__________________________,
你认为还可以作其他何种改进? _____________________________________________。
(2)图二可用于定量比较反应的快慢,检查图二装置气密性的方法是???????????????。
利用图二做实验时需测量的数据是???????????????????????????????。
参考答案:(10分)(每空2分)
(1)反应产生气泡快慢(或反应
本题解析:(1)比较铁盐和铜盐对H2O2分解的催化效果,就是观察产生气泡的快慢;硫酸铜和氯化铁的酸根离子不同,可能影响实验结果,故将酸根离子改成相同的,可以排除酸根对实验结果的影响,
(2)本装置中活塞是活动的,可通过其拉出与推入来改变装置内部的压强,前提关闭A处活塞。
该反应是通过生成气体的反应速率分析判断的,所以根据v=ΔV/Δt来判知,需要测量的数据是产生40ml气体所需要的时间
本题难度:一般
2、选择题 影响化学反应速率的因素很多,下列措施能加快化学反应速率的是 [???? ]
A.升高温度
B.降低温度
C.减小压强
D.降低反应物浓度
参考答案:A
本题解析:
本题难度:一般
3、选择题 100毫升2摩/升H2SO4跟过量锌粉反应,在一定温度下,为了减缓反应进行的速度,但又不影响生成氢气的总量.可向反应物中加入适量的
A.碳酸钠(固体)
B.硝酸钾溶液
C.硫酸钾溶液
D.硫酸铵(固体)
参考答案:C
本题解析:
试题分析:碳酸钠能和稀硫酸反应放出CO2气体,消耗氢离子,降低氢离子的浓度,反应速率降低,但生成的氢气体积减少,A不正确;B中在酸性条件下,硝酸钾具有强氧化性,和锌反应得不到氢气,B不正确;硫酸钾溶液相当于是稀释,氢离子浓度降低,反应速率降低,且生成的氢气体积不变,C正确;硫酸铵固体不能降低氢离子的浓度,所以不能改变反应速率,D不正确,答案选C。
点评:该题是基础性试题的考查,主要是考查学生对外界条件影响反应速率的熟悉了解程度,有利于培养学生的逻辑推理能力,提高学生的应试能力和学习效率。该题
本题难度:一般
4、选择题 足量的Fe粉与一定量的盐酸反应,为了加快反应速率,但又不影响产生氢气的总量,应加入下列物质中的 ( )
A.NaNO3溶液 B.水 C.NaCl固体 D.CuSO4溶液
参考答案:D
本题解析:考查外界条件对反应速率的影响。在酸性溶液中,硝酸钠具有强氧化性,和铁反应生成的表示氢气,而是NO,不正确。B是稀释,降低反应速率。反应的本质是氢离子和铁之间发生的氧化还原反应,所以C是不影响的。加入硫酸铜,铁可以置换出铜,构成原电池,铁是负极,加快反应速率。答案选D。
本题难度:一般
5、选择题 已知汽车尾气无害化处理反应为2NO(g)+2CO(g)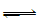 N2(g)+2CO2(g),下列说法中正确的是
N2(g)+2CO2(g),下列说法中正确的是
A.使用适当的催化剂不改变反应速率
B.降低压强能提高反应速率
C.升高温度能提高反应速率
D.改变压强对反应速率无影响
参考答案:C
本题解析:
试题分析:A、使用适当的催化剂可以加快反应速率,错误;B、降低压强,反应速率减慢,错误;C、温度升高,反应速率加快,正确;D、改变压强对反应速率有影响,错误,答案选C。
本题难度:一般