��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �������ʵķ�����ȷ����?????[???? ]
�����??
�����
��
��ʽ��
A.
Ư��??
SO2
��ˮ
NaHCO3
B.
����?
Cl2
KOH
����
C.
����??
HNO3
����
NH4Cl
D.
ʳ��
BaSO4
������
NaHSO3
�ο��𰸣�D
���������
�����Ѷȣ���
2��ѡ���� �������ӷ���ʽ��д��ȷ����
A.�ð�ˮ����������SO2��
B.��˫��ˮ�еμ��������Ը��������Һ����Һ�Ϻ�ɫ��ȥ��
C.�ڼ���������Ũ�����뷴Ӧ��ȡ����������Mn2++Cl2��+2H2O
D.��С�մ���Һ�м��������ʯ��ˮ��
�ο��𰸣�B
���������������A��һˮ�ϰ�Ϊ��������ӷ�Ӧ�б�����ѧʽ��
B������������ԭ��Ӧ���������ӡ�������ˮ��
C����ɺ�Hԭ�Ӿ����غ㣻
D��С�մ���ȫ��Ӧ����Ӧ����̼��ơ�ˮ��NaOH��
���A���ð�ˮ����������SO2�����ӷ�ӦΪ2NH3?H2O+SO2�T2NH4++SO32-+2H2O����A����
B����˫��ˮ�еμ��������Ը��������Һ����Һ�Ϻ�ɫ��ȥ�����ӷ�ӦΪ6H++2MnO4-+5H2O2�TMn2++5O2��+8H2O����ѭ�����غ�������غ㶨�ɣ���B��ȷ��
C����ȡ�������������ӷ�ӦΪ4H++MnO2+2Cl-�TMn2++Cl2��+2H2O����C����
D����С�մ���Һ�м��������ʯ��ˮ�����ӷ�ӦΪCa2++HCO3-+OH-=H2O+CaCO3������D����
��ѡB��
���������⿼�����ӷ�Ӧ����ʽ����д����ȷ�����Ļ�ѧ��Ӧ�ǽ����Ĺؼ���ע�ⷢ����������ԭ��ӦΪ�����ѵ㣬��Ŀ�ѶȲ���
�����Ѷȣ�����
3��ѡ���� ����������ȷ����
A�����ᱵ������ˮ�������ᱵΪ�������
B���������Һ�ܵ��磬���������ҺΪ�����
C��������̼����ˮ�ܲ��ֵ��룬�ʶ�����̼Ϊ�������
D��ʯī���ܵ��磬���Ȳ��ǵ���ʣ�Ҳ���Ƿǵ����
�ο��𰸣�D
���������
���������A�����ᱵ������ˮ��������ˮ�IJ�����ȫ���룬�����ᱵΪǿ����ʣ�����B���������Һ�ܵ��磬���������ҺΪ�����Ȳ��ǵ����Ҳ���Ƿǵ���ʣ�����C��������̼����ˮ��ˮ��Ӧ����̼�ᣬ̼���ܲ��ֵ��룬��̼��Ϊ������ʣ�������̼���ڷǵ���ʣ�����D��ʯīΪ���ʣ�ʯī���ܵ��磬���Ȳ��ǵ���ʣ�Ҳ���Ƿǵ���ʣ���ȷ��
�����Ѷȣ�һ��
4������� �����£���ijһԪ��HA��NaOH��Һ�������ϣ�������Һ��Ũ�Ⱥͻ�Ϻ�������Һ��pH���±�
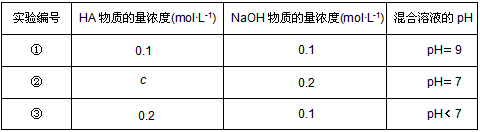
��ش�
��1���Ӣ������������ HA��___________���ǿ�ᡱ�����ᡱ����
��2���������������c___________0.2 (����ڡ�����С�ڡ��� �����ڡ�)�����Һ������Ũ��
c(A-)�� c(Na+)�Ĵ�С��ϵ��___________��
��3�������ڢ���ʵ������˵��HX�ĵ���̶�________NaX��ˮ��̶�(����ڡ���С�ڡ�)���û����Һ������Ũ���ɴ�С��˳����___________��
��4������ʵ�����û����Һ����ˮ�������c(OH-)��___________mol��L-1��
��5��д���û����Һ��������ʽ�ľ�ȷ���(���������Ƽ��㣺)��
c(Na+)��c(A-)��___________mol��L-1��c(OH-)��c(HA)��___________mol��L-1��
�ο��𰸣���1������
��2�����ڣ�c(A-)��c(Na+)
���������
�����Ѷȣ�����
5������� ������������ǿ����ʵ���______�����ڷǵ���ʵ���______���ܵ�������ʵ���______������������ʵ���______��
�ٰ�ˮ��ʳ�ξ�����Ҵ���������Һ��������������ڵ�����آ�������������Һ̬�Ȼ����ʯī��
�ο��𰸣��ٰ�ˮ�ǰ�����ˮ��Һ��ˮ��Һ�ܵ��磬��ˮ�ǻ����Ȳ��ǵ��
���������
�����Ѷȣ�һ��