微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 化学反应N2+3H2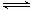 2NH3的能量变化如下图所示,该反应的热化学方程式是
2NH3的能量变化如下图所示,该反应的热化学方程式是
A.N2(g)+3H2(g)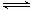 2NH3(1) △H=2(a-b-c)kJ・mol-1
2NH3(1) △H=2(a-b-c)kJ・mol-1
B.N2(g)+3H2(g)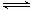 2NH3(g) △H=2(b-a)kJ・mol-1
2NH3(g) △H=2(b-a)kJ・mol-1
C.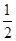 N2(g)+
N2(g)+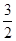 H2(g)
H2(g) 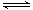 NH3(1) △H=(b+c-a)kJ・mol-1
NH3(1) △H=(b+c-a)kJ・mol-1
D.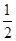 N2(g)+
N2(g)+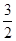 H2(g)
H2(g)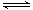 NH3(g) △H=(a+b)kJ・mol-1
NH3(g) △H=(a+b)kJ・mol-1
参考答案:A
本题解析:
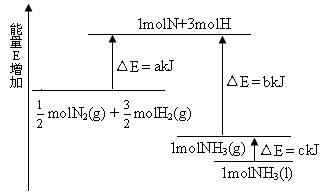
本题较新,也很有特色;重在看清图中标识,找准分子,原子变化过程中相应的能量变化。
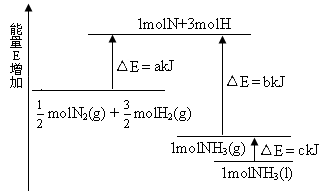
图中a 为反应物键能之和;
图中b 为生成物键能之和;
图中c 为1 mol NH3液化时放出的能量。
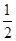 N2(g)+
N2(g)+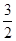 H2(g)
H2(g) 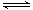 NH3(1) △H=(a-b-c)kJ・mol-1各项同时乘2得
NH3(1) △H=(a-b-c)kJ・mol-1各项同时乘2得
N2(g)+3H2(g)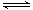 2NH3(1) △H=2(a-b-c)kJ・mol-1
2NH3(1) △H=2(a-b-c)kJ・mol-1
本题难度:一般
2、选择题 下列叙述不正确的是
A.纯银器表面在空气中因化学腐蚀渐渐变暗
B.氢氧燃料电池是一种将化学能转化为电能的装置
C.可用浸有酸性高锰酸钾溶液的滤纸来检验二氧化硫气体的漂白性
D.塑料袋在全球“失宠”,有偿使用成为风尚,是因为塑料袋填埋占用土地,且难以降解
参考答案:C
本题解析:
试题分析:纯银器表面不能构成原电池,因为无活泼性不同的两个电极,因此只可能在空气中发生化学腐蚀而慢慢变暗,故A选项正确;氢氧燃料电池属于化学电源,应用原电池原理,因此能将化学能转化为电能,故B选项正确;酸性高锰酸钾是有颜色的无机物,具有强氧化性,二氧化硫使其紫红色褪色,只能证明二氧化硫的还原性,使有颜色的有机物褪色,发生了非氧化还原反应,才能证明二氧化硫的漂白性,故C选项错误;塑料是合成高分子材料,难以降解,导致白色污染,故D选项正确。
本题难度:简单
3、选择题 已知:(1)H2(g)+1/2O2(g)===H2O(g) ΔH1=a kJ/mol
(2)2H2(g)+O2(g)===2H2O(g) ΔH2=b kJ/mol
(3)H2(g)+1/2O2(g)===H2O(l) ΔH3=c kJ/mol
(4)2H2(g)+O2(g)===2H2O(l) ΔH4=d kJ/mol下列关系式中正确的是 :
A.a<c<0
B.b>d>0
C.2a=b<0
D.2c=d>0
参考答案:C
本题解析:略
本题难度:一般
4、选择题 下列属于放热反应的是
A.石灰石的分解
B.焦炭和二氧化碳共热
C.铝和盐酸反应
D.氯化铵与氢氧化钡反应
参考答案:C
本题解析:
试题分析:石灰石的分解、焦炭和二氧化碳共热、氯化铵与氢氧化钡反应为吸热反应,铝和盐酸反应为放热反应,故答案为C。
考点:本题考查化学反应的热效应。
本题难度:一般
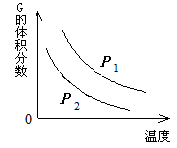
5、选择题 在一密闭容器中有如下反应:L (s) + a G (g)? ?b R (g) 温度和压强对该反应的影响如图所示,其中压强P1 < P2,由此可判断
?b R (g) 温度和压强对该反应的影响如图所示,其中压强P1 < P2,由此可判断
A.正反应为放热反应
B.化学方程式中的计量数a > b
C.G的转化率随温度升高而减小
D.增大压强,容器内气体质量不变
参考答案:B
本题解析:根据图像可知,随着温度的升高,G的体积分数逐渐减小,说明升高温度平衡向正反应方向移动,G的转化率增大,因此正反应是吸热反应,A、C不正确。当温度相同时,压强越大,G的体积分数越小,说明增大压强平衡向正反应方向移动,即正反应是体积减小的,所以a大于b。由于L是固体,向正反应方向移动时,气体的质量是增加的,所以D不正确,B正确,答案选B。
本题难度:一般