微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 (10分)中和热是指酸跟碱发生中和反应生成lmol H2O所放出的热量。某学生想通过测定反应过程中所放出的热量来计算中和热。他将50mL0.5mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应。请回答下列问题:
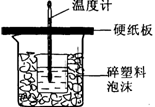
(1) 从实验装置上看,图中尚缺少的一种玻璃用品是__________________;装置的不足之处是??????????;不加以改正,所求的值将 ?????????????(填偏大,偏小,无影响)。
(2) 实验中改用60 mL 0.50 mol/L的盐酸跟50mL 0.55 mol/L的NaOH溶液进行反应,与上述实验相比,所放出的热量________(填“相等”或“不相等”);所求中和热的数值会________(填“相等”或“不相等”)。
参考答案:(1)环形玻璃搅拌棒;大烧杯没有和小烧杯在同一水平面上;偏小
本题解析:考查中和热的测定。在实验中为了使溶液混合均匀,需要搅拌,因此还需要环形玻璃搅拌棒。为了减少热量的损失,2个烧杯的口径应该水平,在一条线上。由于装置中小烧杯的口径靠下,使得一部分热量损失,测定的中和热偏小。当改变酸或碱的用量时,反应中放出的热量会发生变化,但中和热是不变的。
本题难度:简单
2、选择题 下列关于热化学反应的描述中正确的是??????????? ( )
A.已知H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ・mol-1,则H2SO4和Ba(OH)2反应的反应热ΔH=2×(-57.3) kJ・mol-1
B.燃料电池中将甲醇蒸气转化为氢气的热化学方程式是CH3OH(g)+ O2(g)===CO2(g)+2H2(g)ΔH=-192.9 kJ・mol-1,则CH3OH(g)的燃烧热为192.9 kJ・mol-1
O2(g)===CO2(g)+2H2(g)ΔH=-192.9 kJ・mol-1,则CH3OH(g)的燃烧热为192.9 kJ・mol-1
C.H2(g)的燃烧热是285.8 kJ・mol-1,则2H2O(g)===2H2(g)+O2(g) ΔH=571.6 kJ・mol-1
D.葡萄糖的燃烧热是2 800 kJ・mol-1,则 C6H12O6(s)+3O2(g)===3CO2(g)+3H2O(l) ΔH=-1 400 kJ・mol-1
C6H12O6(s)+3O2(g)===3CO2(g)+3H2O(l) ΔH=-1 400 kJ・mol-1
参考答案:D
本题解析:
试题分析:A、中和热是指稀溶液中,强酸和强碱发生中和反应生成1molH2O所放出的热量,生成2molH2O所放出的热量为2×57.3kJ,但生成硫酸钡沉淀的反应还要吸收热量,则H2SO4和Ba(OH)2反应的反应热小于2×(-57.3)kJ?mol-1,故A错误;B、由燃烧热的概念可知,甲醇燃烧应生成液态水,则CH3OH的燃烧热一定不为192.9kJ?mol-1,故B错误;C、H2(g)的燃烧热是285.8kJ?mol-1,生成液态水,则2H2O(l)=2H2(g)+O2(g) △H=+571.6
本题难度:一般
3、选择题 在测定中和热的实验中,下列说法正确的是
A.使用环形玻璃搅拌棒是为了加快反应速率,减小实验误差
B.为了准确测定反应混合溶液的温度,实验中温度计水银球应与小烧杯底部接触
C.用0.5mol・L-1NaOH溶液分别与0.5 mol・L-1的盐酸、醋酸溶液反应,如所取的溶液体积相等,则测得的中和热数值相同
D.在测定中和热实验中需要使用的仪器有:天平、量筒、烧杯、滴定管、温度计
参考答案:A
本题解析:A正确,搅拌可加快反应速率,减小热量损耗;B错,实验中温度计水银球不能与小烧杯底部接触;C错,盐酸为强酸而醋酸为弱酸,弱酸电离要吸收能量,两者所测中和热数值不同;D错,在测定中和热实验中没有使用到天平;
本题难度:一般
4、选择题 化学反应A2+B2=2AB的能量变化如图所示,则下列说法正确的是( )

A.该反应是吸热反应
B.断裂1 mol A―A键和1 mol B―B键能放出x kJ的能量
C.断裂2 mol A―B键需要吸收y kJ的能量
D.2 mol AB的总能量高于1 mol A2和1 mol B2的总能量
参考答案:C
本题解析:根据图像可知,反应物的总能量高于生成物的总能量,所以是放热反应。由于断键是吸热的,形成化学键是放热的,所以只有选项C是正确的,其余都是错误的,答案选C。
本题难度:简单
5、选择题 下列有关能量变化说法正确的是(???)。
A.化学反应除了生成新物质外,还伴随着能量的变化
B.放热反应都不需要加热就可以发生
C.需要加热的化学反应都是吸热反应
D.化学反应放热还是吸热,取决于反应条件
参考答案:A
本题解析:反应是放热反应,还是吸热反应与反应条件是无关系的,只与反应物总能量和生成物总能量的相对大小有关系,因此选项B、C、D都是错误的,只有选项A是正确的,答案选A。
本题难度:一般