微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (14分)为了减少煤燃烧对大气造成的污染,煤的气化和液化是高效、清洁利用煤炭的重要途径,而减少CO2气体的排放也是人类面临的重大课题.煤综合利用的一种途径如下所示:
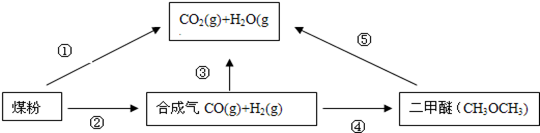
(1)已知:C(s)+H2O(g)====CO(g)+H2(g) △H1=+131.3kJ?mol-1
C(s)+2H2O(g)====CO2(g)+2H2(g) △H2=+90kJ?mol-1
则一氧化碳与水蒸气反应生成二氧化碳和氢气的热化学方程式是 。
(2)将燃煤废气中的CO2转化为二甲醚的反应原理为:2CO2(g)+6H2(g)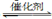 CH3OCH3(g)+3H2O(g);ΔH
CH3OCH3(g)+3H2O(g);ΔH
①该反应平衡常数表达式为K= 。
②已知在某压强下,该反应在不同温度、不同投料比时,CO2的转化率如图所示。
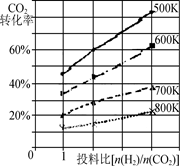
该反应的ΔH________(填“>”、“<”或“=”)0。若温度不变,减小反应投料比[n(H2) /n(CO2)],则K将________(填“增大”、“减小”或“不变”)。
(3)一种新型氢氧燃料电池工作原理如下图所示。
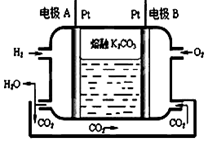
①写出电极A的电极反应式 放电过程中,溶液中的CO32-将移向电极 (填A或B)
②以上述电池电解饱和食盐水,若生成0.2mol Cl2,则至少需通入O2的体积为 L(标准状况)
2、选择题 一定条件下,可逆反应N2+3H2 2NH3(正反应为放热反应)达到平衡,当单独改变下述条件后,有关叙述错误的是[???? ]
2NH3(正反应为放热反应)达到平衡,当单独改变下述条件后,有关叙述错误的是[???? ]
A.加催化剂,V正、V逆都发生变化,且变化的倍数相等
B.加压,V正、V逆都增大,且V正增大的倍数大于V逆增大的倍数
C.降温,V正、V逆都减小,且V正减小的倍数大于V逆减小的倍数
D.增大氮气的浓度,N2转换率减小,H2转化率增大
3、填空题 (16分)在450℃并有催化剂存在下,在体积为1L的密闭恒温容器中,二氧化硫和氧气发生如下反应:2SO2+ O2  2SO3
2SO3
(1)已知:64g SO2完全转化为SO3会放出85kJ热量。 SO2转化为SO3的热化学方程式是 。
(2)该反应的化学平衡常数表达式K= 。
(3)降低温度,化学反应速率 。该反应K值将 。(填“增大”或“减小”或“不变”)
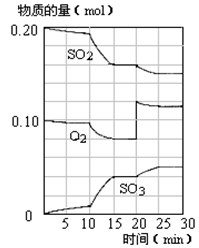
(4)450℃时,在一密闭容器中,将二氧化硫与氧气混合,反应过程中SO2、O2、SO3物质的量变化如图,反应处于平衡状态的时间段是 。
a.10-15min b.15-20min c.20-25min d.25-30min
(5)据图判断,10min到15min的曲线变化的原因可能是 (填写编号)。
a.增加SO3的物质的量 b.增大容器体积 c.降低温度 d.催化剂
(6)在15分钟时,SO2的转化率是 。
4、选择题 压强变化不会使下列化学反应的平衡发生移动的是
[???? ]
A.H2(g)+ I2(g)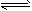 2HI(g)
2HI(g)
B.3H2(g)+N2(g)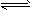 2NH3(g)
2NH3(g)
C.2SO2(g)+O2(g)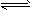 2SO3(g)
2SO3(g)
D.C(s)+CO2(g)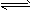 2CO(g)
2CO(g)
5、简答题 800℃时,在2L密闭容器内,发生反应:2NO(g)+O2(g)?2NO2(g),已知在此体系中,n(NO)随时间的变化如表:
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5
n(NO)(mol)
0.020
0.01
0.008
0.007
0.007
0.007
(1)已知升高温度,NO2的浓度减小,则该反应是______(填“吸”或“放”)热反应.
(2)该反应平衡常数K的表达式为______
(3)如图中表示NO2的变化的曲线是______用O2表示从0~2s内该反应的平均速率v=______
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的是______
a.及时分离除NO2气体????b.适当升高温度
c.增大O2的浓度?????????d.选择高效催化剂.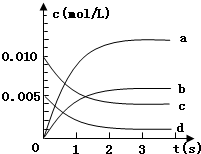
|