微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列说法错误的是
[???? ]
A.蒸馏时应调整温度计的水银球于蒸馏烧瓶支管口附近
B.提纯液体混合物常用重结晶法
C.萃取是利用溶质在两种互不相溶的溶剂中溶解度的不同,使溶质从一种溶剂内转移到另一种溶剂的操作。
D.常用质谱法进行有机物相对分子质量的测定
参考答案:B
本题解析:
本题难度:一般
2、填空题 氢溴酸在医药和石化工业上有广泛用途。下图是模拟工业制备氢溴酸粗品及精制的流程:
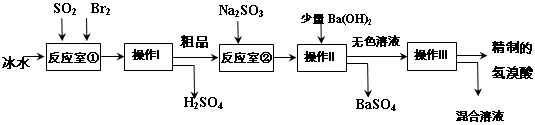
已知:Br2是易挥发、深红棕色的液体;氢溴酸是易挥发、无色液体。
根据上述流程回答下列问题:
(1)反应室①中发生反应的化学方程式为??????????????。
(2)反应室①使用冰水的目的???????????。
(3)操作I的名称??????????,操作Ⅱ用到的玻璃仪器有???????????。
(4)反应室②中加入Na2SO3的目的是?????????????。
(5)工业生产中制得的氢溴酸带有淡淡的黄色。于是甲乙两同学设计了实验加以探究:
①甲同学假设工业氢溴酸呈淡黄色是因为含Fe3+,则用于证明该假设所用的试剂为 ??????????,若假设成立可观察到的现象为???????????。
②乙同学假设工业氢溴酸呈淡黄色是因为????????,其用于证明该假设成立的方法为 ?????????????。
参考答案:(1)SO2+Br2+2H2O=H2SO4+2HBr??(2
本题解析:
试题分析:(1)反应室①中SO2和Br2在冰水中发生反应的化学方程式为SO2+Br2+2H2O=H2SO4+2HBr。(2)反应室①使用冰水的目的是为了防止Br2和HBr挥发而污染空气,影响操作。(3)操作I是分离互溶的沸点不同的液体物质的操作。名称是蒸馏。操作Ⅱ用到的玻璃仪器有漏斗、玻璃棒、烧杯。(4)反应室②中加入Na2SO3的目的是为了消耗为反应的Br2,提高物质的纯度。(5)工业生产中制得的氢溴酸带有淡淡的黄色。①甲同学假设工业氢溴酸呈淡黄色是因为含Fe3+。检验的方法是取少量的溶液,向其中滴加几滴KSCN溶液,若工业氢溴酸遇KSCN溶液变红色;就证明含有Fe3+;否则就吧含有Fe3+。②乙同学假设工业氢溴酸呈淡黄色是因为含有Br2。检验的方法是利用其强氧化性。用玻璃棒蘸取制得的氢溴酸,点在湿润淀粉KI试纸上变蓝(也可以利用其在有机溶剂中的溶解度大的性质。用胶头滴管取制得的氢溴酸于试管中,滴加CCl4、振荡、静止,下层呈橙红色),证明因含Br2而显黄色。2和Br2的性质、混合物的分离方法、操作、Fe3+和Br2的检验方法的知识。
本题难度:一般
3、选择题 除去混入NO 中的少量NO2应将气体通过下列试剂中的[???? ]
A 、Na2CO3(aq )
B 、NaHCO3(aq )
C 、H2O
D 、浓H2SO4
参考答案:C
本题解析:
本题难度:简单
4、选择题 下列离子检验的方法正确的是
A.某溶液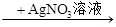 生成白色沉淀,说明原溶液中有Cl-
生成白色沉淀,说明原溶液中有Cl-
B.某溶液 生成白色沉淀,说明原溶液中有SO42-
生成白色沉淀,说明原溶液中有SO42-
C.某溶液 生成红褐色沉淀,说明原溶液中有Fe3+
生成红褐色沉淀,说明原溶液中有Fe3+
D.某溶液 生成无色气体,说明原溶液中有CO32-
生成无色气体,说明原溶液中有CO32-
参考答案:C
本题解析:
试题分析:A、CO32?、SO32?等离子也能与Ag+反应生成白色沉淀,错误;B、能与BaCl2反应生成白色沉淀的除了SO42?还有CO32?、SO32?等离子,错误;C、能与NaOH溶液反应生成红褐色沉淀的只有Fe3+,正确;D、能与稀硫酸反应生成无色气体的离子除了CO32?还有HCO3?、SO32?、HSO3?等,错误。
本题难度:一般
5、填空题 怎样除去苯中混有的苯酚?????????????????????????????????????????????????
参考答案:在溶液中加NaOH溶液,再分液。
 本题解析:在溶液中加入溴水,再过滤除去生成的三溴苯酚即可。
本题解析:在溶液中加入溴水,再过滤除去生成的三溴苯酚即可。
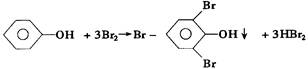
事实上,三溴苯酚为白色不溶于水的沉淀,却溶于有机物苯中,根本不能过滤出来。正确的解法:在溶液中加NaOH溶液,再分液。
本题难度:一般