微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力I随加入水的体积V变化的曲线如图所示。
请回答:
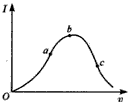
(1)“O”点导电能力为O的理由是___;
(2)a、b、c三点溶液中c(H+)由小到大的顺序为____,
(3)a、b、c三点中醋酸电离度最大的是____;水电离程度最大的是____。
(4)若使c点溶液的c(CH3COO-)提高,在如下措施中可采取___(填标号)。
A.加盐酸
B.加冰醋酸
C.加入固体KOH
D.加水
E.加固体CH3COONa
F.加Zn粒
参考答案:(1)此时加水为零,醋酸没有电离,以醋酸分子的形式存在
本题解析:
本题难度:一般
2、选择题 下列事实中,能证明硫酸是强酸的是?(???)
A.能使石蕊试液变红
B.能跟锌反应产生氢气
C.1 mol/L 硫酸溶液中H+浓度为2 mol/L
D.能与碳酸钠反应放出二氧化碳气体
参考答案:C
本题解析:
试题分析:A、B都只能说明硫酸显酸性,但不能说明硫酸是强酸。D说明硫酸但酸性强于碳酸,不能说明硫酸是强酸。1 mol/L 硫酸溶液中H+浓度为2 mol/L,说明硫酸在溶液中完全电离出氢离子,是强酸,答案选C。
点评:该题是中等难度的试题,试题贴近高考,注重能力的培养。有助于培养学生的逻辑思维能力和发散思维能力,提高学生灵活运用基础知识解决实际问题的能力。
本题难度:一般
3、选择题 在-50℃时,液氨的电离跟水的电离相似,存在平衡,2NH3(l)?N
H
+4
+NH
-2
,NH
+4
的平衡浓度为1×10-15mol?L-1,下列说法错误的是( )
A.在液氨中加入NaNH2,可使液氨的离子积变大
B.在液氨中加入NH4Cl,液氨的离子积不变
C.此温度下液氨的离子积K为1×10-30
D.在液氨中加入金属钠可能有NaNH2生成
参考答案:A、虽然加入NaNH2可使平衡向逆反应方向移动,NH2-的浓
本题解析:
本题难度:简单
4、选择题 分别在等体积等pH或等物质的量浓度的盐酸和醋酸溶液中,加入足量锌粉,氢离子浓度c(H+)及氢气的体积V(H2)(同温同压下测定)的变化图示如下,其中正确的是? (?? )
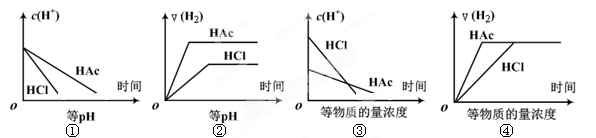
A.①②③
B.②④
C. ①③
D.①②③④
参考答案:A
本题解析:
试题分析:①随着反应的进行,氢离子浓度逐渐减小但是醋酸会逐渐电离出氢离子,所以醋酸中氢离子消耗的速率慢,正确;②等pH时,醋酸浓度较大,加入足量锌,不仅产生的氢气的体积更大,而且反应更快,正确;③等浓度的盐酸和醋酸,盐酸的pH小,和金属锌反应的速率比醋酸的快正确;④等浓度的盐酸和醋酸,因为盐酸是强酸,醋酸是弱酸,盐酸中H+浓度大,和金属锌反应的速率是盐酸比醋酸的快,错误,故A项正确。
本题难度:一般
5、简答题 (2009?江门一模)某二元酸(H2A?)在水中的电离方程式:H2A=H++HA-,HA-?H++A2-H+又知0.lmol?L-1NaHA溶液的pH=2,下列说法不正确的是( )
A.因为A2-+H2O?HA-+OH-,所以Na2A溶液显碱性
B.0.lmol?L-1H2A溶液中氢离子的物质的量浓度为0.11?mol?L-1
C.NaHA溶液中各种离子浓度的关系是c?(Na+)>c?(HA-)>c(H+)>c?(A2-)>c?(OH-)
D.在NaHA溶液中,HA-电离的趋势大于其水解的趋势
参考答案:A.因为A2-弱酸根离子,则Na2A溶液显碱性是因A2-+H
本题解析:
本题难度:一般
网站客服QQ: 960335752 - 14613519 - 791315772