微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 关于原电池的叙述中正确的是?????????????????????????????????????????
A.构成原电池的电极是两种不同的金属
B.原电池是将化学能转化为电能的装置
C.原电池负极发生的电极反应是还原反应
D.原电池的正极是还原剂,总是溶液中的阳 离子在此被还原
离子在此被还原
参考答案:B
本题解析:略
本题难度:简单
2、选择题 高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为:
3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH
3Zn(OH)2+2Fe(OH)3+4KOH
下列叙述不正确的是(??)
A.放电时负极反应为:Zn-2e-+2OH-=Zn(OH)2
B.放电时正极反应为:FeO42-+4H2O+3e-=Fe(OH)3+5OH-
C.放电时每转移3 mol电子,正极有1 mol K2FeO4被氧化
D.放电时正极附近溶液的碱性增强
参考答案:C
本题解析:高铁电池放电时为原电池,依据原电池工作原理,放电时负极反应式为Zn-2e-+2OH-=Zn(OH)2,用总式减去负极反应式即得正极反应式为:FeO42-+4H2O+3e-=Fe(OH)3+5OH-,放电时每转移3 mol电子,正极有1 mol K2FeO4被还原。
本题难度:一般
3、选择题 目前已研制成功多种锂电池。某种锂电池的总反应式为Li+MnO2=LiMnO2,下列说法正确的是(? )。
A.Li是正极,电极反应为Li-e-=Li+
B.Li是负极,电极反应为Li-e-=Li+
C.Li是负极,电极反应为MnO2+e-=Mn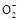
D.Li是负极,电极反应为Li-2e-=Li2+
参考答案:B
本题解析:本题根据总反应式判断Li被氧化,为负极材料,失去电子成为Li+,正极放电的为MnO2,若已知电池总反应式而要写电极反应式,这类题的一般处理方法是:根据“负失氧、正得还”的规律先判断出负极材料,负极材料若是金属,则失电子而变为相应阳离子(注意:Fe失电子应变为Fe2+),负极材料若是其他被氧化的物质(如氢氧燃料电池中的H2、甲烷燃料电池中的CH4),则失电子变为相应氧化产物,然后再推断正极反应。
本题难度:一般
4、填空题 利用反应:Fe+2Fe3+=3Fe2+制一个化学电池(给出若干导线和一个小灯泡,电极材料和电解液自选),画出实验装置图,注明电解质溶液名称和正负极材料,标出电子流动方向和电流方向,写出其电极反应式。_______________________________________
参考答案:Cu是正极,正极反应式:2Fe3++2e-=2Fe2+;Fe
本题解析:
本题难度:一般
5、选择题 铜片和锌片用导线连接后插入稀硫酸中,锌片为[???? ]
A.阴极
B.正极
C.阳极
D.负极
参考答案:D
本题解析:
本题难度:简单