微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (1) ( 6分) 书写下列离子方程式:
实验室制取CO2 ___ ___________________________________________________________________
___________________________________________________________________
硫酸铜溶液与氢氧化钡溶液_____________________________________
CO2 通入足量氢氧化钠_______________________________________
通入足量氢氧化钠_______________________________________
(2)(4分)写出下列物质的电离方程式:
NaHSO4 _______,
H2CO3 ________。
参考答案:略
本题解析:略
本题难度:一般
2、选择题 下列离子方程式正确的是( )
A.澄清的石灰水与稀盐酸反应Ca(OH)2+2H+=Ca2++2H2O
B.硫酸铜溶液与氢氧化钡溶液反应 :Ba2++ SO42
参考答案:
本题解析:
本题难度:简单
3、选择题 下列反应的离子方程式书写正确的是
A.钠和冷水反应:Na+2H2O==Na++2OH―+H2↑
B.金属铝溶于氢氧化钠溶液:Al+2OH―==AlO2―+H2↑
C.向Al2(SO4)3溶液中加入过量的氨水:Al3++3NH3・H2O =Al(OH)3↓+ 3NH4+
D.少量SO2通入漂白粉溶液中:SO2+H2O+Ca2++2ClO-===CaSO3↓+2HClO
参考答案:C
本题解析:
试题分析:A项钠和冷水反应:2Na+2H2O==2Na++2OH―+H2↑,故A项错误;B项金属铝溶于氢氧化钠溶液:2Al+2H2O+2OH―==2AlO2―+3H2↑,故B项错误;D项HClO具有强氧化性,+4价S具有还原性,故应发生氧化还原反应,故D项错误;C项离子方程式书写正确,本题选C。
考点:离子方程式判断正误。
本题难度:一般
4、选择题 下列离子方程式书写正确的是
A.在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:
3ClO―+Fe(OH)3= FeO42―+3Cl―+H2O+4H+
B.用Na2O2与H2O反应制备O2:Na2O2+ H2O=2Na++2OH-+ O2↑
C.向Fe(NO3)2溶液中加入过量的HI溶液 3Fe2++NO-3+4H+-=3Fe3++NO↑+2H2O
D.将等体积等物质的量浓度的NaHCO3溶液与Ba(OH)2溶液混合
HCO-3+Ba2++OH-=BaCO3↓+H2O
参考答案:D
本题解析:略
本题难度:一般
5、填空题 氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质。为了提纯氯化钾,先将样品溶于适量水中,充分搅拌后过滤,再将滤液按如下图所示步骤进行操作(注意事项:①所加试剂必须过量;②过量试剂必须除去;③不能引入新的杂质)。
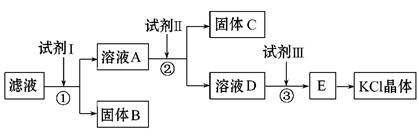
回答下列问题:
(1)试剂Ⅰ的化学式为 ,①中发生反应的离子方程式为
。
(2)试剂Ⅱ的化学式为 ,②中加入试剂Ⅱ的目的是 。
(3)试剂Ⅲ的名称是 ,③中发生反应的离子方程式为 。
(4)某同学称取提纯的产品0.775 9 g,溶解后定容在100 mL容量瓶中,每次取25.00 mL溶液,用硝酸银溶液反应共消耗硝酸银0.002 562 mol,则该产品的纯度为
。
参考答案:(1)BaCl2  本题解析:
本题解析:
试题分析:(1)要除掉杂质离子硫酸根离子和碳酸根离子,应加入过量的钡离子,又不能引入其他离子,因此选用BaCl2溶液,与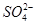 和
和 均能反应。
均能反应。
(2)要除掉多余的钡离子,所需试剂必须既能除去过量的Ba2+,又不能引入其他杂质且过量离子较易除去,因此选用K2CO3。
(3)要除掉多余的碳酸根离子,要滴加过量的盐酸。
(4)硝酸银的物质的量就是氯化钾的物质的量,则纯度为0.002 562×74.5×4÷0.775 9=0.984 0;另外从本题所给数据来看需保留四位有效数字。
考点:常见物质的检验、分离和提纯,化学计算
本题难度:一般