微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 某研究小组采用往一定体积的食醋中滴入已知浓度的NaOH溶液的方法测定食醋中醋酸的浓度.下列说法正确的是
A.滴定时,使用酚酞作指示剂,溶液颜色恰好由无色变为浅红色,且半分钟内不褪色时,为滴定终点
B.滴定时眼睛要注视着滴定管内NaOH溶液的液面变化,防止滴定过量
C.碱式滴定管若滴定前平视读数、滴定后俯视读数,则测定结果偏高.
D.酸式滴定管用水洗净后未用食醋润洗,则测得的食醋浓度偏高
2、简答题 滴定法是化学定量分析的一种重要而普遍的方法.
I:如图是常温下用0.1000mol?L-1NaOH溶液滴定20.00mL0.1000mol?L-1某一元酸HX溶液所得滴定曲线.
请回答下列问题:
(1)若学生分组实验需用约400mL0.1000mol?L-1NaOH溶液,配制所需溶液时必需的定量玻璃仪器是______.
(2)判断HX是______(填“强酸”或“弱酸”),理由是______
(3)点①所示溶液中,各离子浓度由大到小的顺序是______.
II:某校化学探究小组用高锰酸钾滴定法测定市场上某品牌钙补品中钙的含量.测定的步骤如下:
①取10.00mL样品,加入适量盐酸酸化,再加入足量的沉淀剂草酸铵[(NH4)2C2O4]溶液,然后慢慢滴加氨水,并调节溶液pH至3.5~4.5之间,产生草酸钙沉淀;
②将沉淀放置过夜或加热半小时使沉淀陈化,过滤、洗涤;
③将洗净的沉淀溶解于适量稀硫酸中,加热至75℃~85℃,用0.1000mol?L-1高锰酸钾溶液滴定至终点,记录消耗的高锰酸钾溶液体积;
④重复上述①~③操作,有关数据记录如表.
实验
样品体积/mL
高锰酸钾溶液体积/mL
1
10.00
8.98
2
10.00
8.58
3
10.00
9.02
4
10.00
9.00
(1)判断滴定终点的现象是______.
(2)写出滴定时所发生反应的离子方程式______.
(3)计算样品中钙的含量______g/L.
(4)下列操作会使测量结果偏低的是______.
a.滴定前俯视读数,滴定后仰视读数
b.滴定过程中,不慎将锥形瓶中少量待测液体摇出瓶外
c.滴定前酸式滴定管尖嘴部分有气泡,滴定后尖嘴部分充满溶液
d.沉淀溶解于稀硫酸时,滤纸上仍残留少量固体.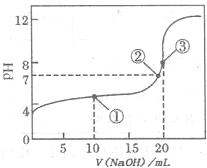
3、选择题 当用酸滴定碱时,下列操作中会使测定结果(碱的浓度)偏低的是???[???? ]
A.酸式滴定管滴至终点后,俯视读数
B.碱液移入锥形瓶后,加了10mL蒸馏水在滴定
C.酸式滴定管用蒸馏水润洗后,未用标准液润洗
D.酸式滴定管注入酸液后,尖嘴留有气泡即开始滴定,滴定终点时气泡消失
4、简答题 用中和滴定法确定某烧碱样品的浓度,试根据实验回答下列问题:
(1)准确称取一定量的样品,配成500mL待测溶液.称量时,样品可放在______(填编号字母)上称量
(A)小烧杯?????(B)洁净纸片???(C)直接放在托盘上
(2)滴定时,用0.20mol?L-1的盐酸来滴定待测溶液,不可选用______(填编号字母)作指示剂.
(A)甲基橙?????(B)石蕊???????(C)酚酞
(3)若选用酚酞作指示剂,用0.20mol?L-1的盐酸来滴定待测溶液,滴定终点的判断依据是______,此时溶液显______性.
(4)根据下表数据,计算被测烧碱溶液的物质的量浓度是______mol?L-1.
| 滴定次数 | 待测溶液体积(mL) | 标准酸体积
滴定前的刻度(mL)
滴定后的刻度(mL)
第一次
10.00
0.40
20.50
第二次
10.00
4.10
24.00
第三次
10.00
0.40
21.50
(5)下列实验操作会对滴定结果产生的后果.(填“偏高”、“偏低”或“无影响”)
①观察酸式滴定管液面时,开始俯视,滴定终点平视,则滴定结果______.
②若将锥形瓶用待测液润洗,然后再加入10.00mL待测液,则滴定结果______.
③若烧碱溶液隔夜后滴定,选用甲基橙作指示剂时,则滴定结果______.
5、实验题 某学生用0.2000mol・L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作为如下几步:
① 用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至0刻度线以上
② 固定好滴定管并使滴定管尖嘴充满液体
③ 调节液面至0或0刻度线稍下,并记下读数
④ 移取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液
⑤ 用标准液滴定至终点,记下滴定管液面读数。
请回答:
(1)以上步骤有错误的是(填编号)____________,该错误操作会导致测定结果___________(填“偏大”、“偏小”或“无影响”)
(2)步骤⑤中,在记下滴定管液面读数时,滴定管尖嘴有气泡,将导致测定结果____________(填“偏大”、“偏小”或“无影响”)
(3)判断滴定终点的现象是:____________________
(4)图26是某次滴定时的滴定管中的液面,其读数为________________mL

(5)根据下列数据:请计算待测盐酸溶液的浓度:________________
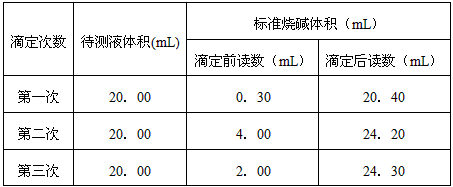
|