微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列实验操作与安全事故处理均正确的是(????)
①做银镜反应实验后的试管内壁附有银,可用氨水清洗
②配制一定物质的量浓度的NaCl溶液时,只需使用1次玻璃棒
③欲从碘水中分离出I2,可将适量的CCl4加入碘水中振荡静置分层后分液
④将饱和氯化铁溶液煮沸,可制 得氢氧化铁胶体
⑤使用水银温度计测量烧杯中水浴温度时,不慎打破水银球,用滴管将水银吸出放入水封的小瓶中,残破的温度计插入装有硫粉的广口瓶中
⑥用试管夹从试管底由下往上夹住距试管口约1/3处,手持试管夹长柄末端,进行加热
⑦制备乙酸乙酯时,将乙醇和乙酸依次加入到浓硫酸中
⑧把玻璃管插入橡胶塞孔时,用厚布护手,紧握用水湿润的玻璃管插入端,缓慢旋进塞孔中
A.①③④⑥??????? B.②⑤⑥⑦????? ③⑤⑥⑧?????? D.⑤⑥⑦⑧
③⑤⑥⑧?????? D.⑤⑥⑦⑧
参考答案:
C
本题解析:略
本题难度:简单
2、选择题 下列实验装置或操作正确的是
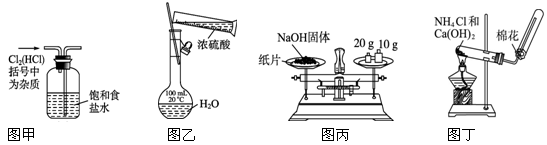
A.图甲:除去Cl2中混有的HCl
B.图乙:用浓硫酸配制一定浓度的稀硫酸
C.图丙:称量氢氧化钠固体
D.图丁:实验室制备氨气
参考答案:D
本题解析:
试题分析:A项洗气瓶中导管应该“长进短出”,错误;B项不能在容量瓶中直接稀释浓硫酸,错误;C项称量氢化钠固体时,氢氧化钠固体有腐蚀性应该放在小烧杯中进行称量,错误。
本题难度:一般
3、选择题 要配制物质的量浓度为1.0 mol・L-1 的NaOH溶液100mL,需要使用的是
A.50mL容量瓶
B.100mL容量瓶
C.250mL容量瓶
D.500mL容量瓶
参考答案:B
本题解析:容量瓶应该选用配制所需体积规格的,如没有选用比配制体积大的容量瓶。
本题难度:一般
4、实验题 Ⅰ、高纯MnCO3是制备高性能磁性材料的主要原料。实验室以MnO2为原料制备少量高纯MnCO3的操作步骤如下:
(1)制备MnSO4溶液:在烧瓶中(装置见图)加入一定量MnO2??和水,搅拌,通入 SO2和N2混合气体,反应3h。停止通入SO2,继续反应片刻,过滤(已知MnO2+H2SO3=MnSO4+H2O)。
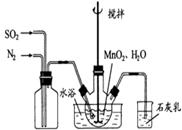
①石灰乳作用:?????????????????????????。
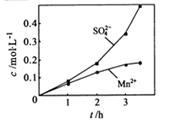
②若实验中将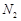 换成空气,测得反应液中Mn2+、SO42-的浓度随反应时间t变化如右图。导致溶液中Mn2+、SO42-浓度变化产生明显差异的原因是???????????????????????????????。
换成空气,测得反应液中Mn2+、SO42-的浓度随反应时间t变化如右图。导致溶液中Mn2+、SO42-浓度变化产生明显差异的原因是???????????????????????????????。
(2)制备高纯MnCO3固体:已知MnCO3难溶于水、乙醇,潮湿时易被空气氧化,100℃开始分解;Mn(OH)2开始沉淀时pH="7.7," 请补充由(1)制得的MnSO4溶液制备高纯MnCO3的操作步骤:
[实验中可选用的试剂:Ca(OH)2、NaHCO3、Na2CO3、C2H5OH]。
①???????????????????????????????????????????????;
②??????????????????????????????????????????????;????
③检验SO42-是否被洗涤除去;?????④用少量乙醇洗涤;?????????⑤低于100℃干燥。
Ⅱ、锌铝合金的主要成分有Zn、Al、Cu、Si等元素。实验室测定其中Cu含量的步骤如下:①称取该合金样品1.1g,用HCl和H2O2溶解后,煮沸除去过量H2O2,过滤,滤液定容于250mL容量瓶中。
②用移液管移取50.00mL滤液于250mL碘量瓶中,控制溶液的pH=3~4,加入过量KI溶液(生成CuI和I2)和指示剂,用0.01100mol×L-1Na2S2O3溶液滴定生成的I2至终点(反应:I2 + 2S2O32- = 2I- + S4O62-),消耗Na2S2O3溶液6.45mL。
(1)判断步骤②滴定终点的方法是???????????????????????????????????????????????。
(2)计算合金中Cu的质量分数??????????????。
参考答案:Ⅰ、(1)①吸收多余的二氧化硫(1分)②O2与H2SO3反应
本题解析:Ⅰ、(1)①由于SO2是大气污染物,需要尾气处理,即石灰乳的作用是吸收多余的二氧化硫。
②由于氧气具有氧化性,而亚硫酸具有还原性,因此原因是O2与H2SO3反应生成H2S04导致的。
(2)要生成碳酸锰,则需要加入碳酸盐,然后通过控制溶液的pH即可产生碳酸锰。碳酸锰不溶于水,过滤得到,即步骤是①边搅拌边加入NaHCO3(Na2CO3),并控制溶液pH<7.7 (2分)②过滤,用少量水洗涤2~3次。
Ⅱ、(1)①由于碘遇淀粉显蓝色,所以指示剂是淀粉,终点时的现象是当滴入最后一滴Na2S2O3溶液时,溶液由蓝色突变为无色,且半分钟不变色。
②铜离子氧化碘离子的方程式为2Cu2++4I-=2CuI+I2,因此根据I2 + 2S2O32- = 2I- + S4O62-可知,Cu2+~S2O32-。所以铜离子的物质的量是0.01100mol/L×0.00645L=7.095×10-5mol,则合金中铜的质量是7.095×10-5mol×5×64g/mol=0.022704g,所以质量分数是0.022704÷1.1=0.02064。
本题难度:一般
5、选择题 下列实验操作中,错误的是??????????????????????????????????(????)???????????????????????????????????????
A.蒸发操作时,不能使混合物中的水分完全蒸干后,才停止加热
B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
C.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
D.萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
参考答案:D
本题解析:D错,萃取操作时,对于萃取剂要求:1、萃取剂与原溶剂不反应;2、萃取剂与原溶液互不相溶;3、溶质在萃取剂中的溶解度远大于在原溶剂中的溶解度;
本题难度:简单