微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列有关说法正确的是????????????????????????????????(??)
A.TATP(C8H18O6)受撞击分解爆炸,且无明显热效应,说明该分解反应熵显著增加
B.NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同
C.pH=3的盐酸与pH=11的LiOH溶液等体积混合溶液呈碱性,说明LiOH为强碱
D.Na2CO3溶液中加入少量Ca(OH)2固体,CO32-水解程度减小,溶液的pH减小
参考答案:A
本题解析:
试题分析:A、根据△G=△H―T・△S可知,△G<0时反应自发。如果TATP(C8H18O6)受撞击分解爆炸,且无明显热效应,说明该分解反应熵显著增加,即△S>0,A正确;B、氯化钠是强酸强碱盐,不水解,溶液显中性。醋酸铵是弱酸弱碱盐,酸根离子与铵根离子水解程度相同,溶液显中性,但促进水的电离,B不正确;C、pH=3的盐酸与pH=11的LiOH溶液等体积混合溶液呈碱性,说明LiOH为弱碱,碱过量,溶液显碱性,C不正确;D、Na2CO3溶液中加入少量Ca(OH)2固体生成碳酸钙沉淀和氢氧
本题难度:一般
2、选择题 下列说法不正确的是
A.0.1mol/L硫酸铵溶液中各离子的浓度由大到小的顺序是:c (NH4+)>c(SO42-)>c(H+)>c(OH-)
B.在苏打与小苏打的混合溶液中存在:c(Na+)+c(H+) ="c(OH" -)+2c(CO32-)+c(HCO3-)
C.在滴有酚酞的Na2CO3溶液中,加入BaCl2溶液后红色褪去,证明Na2CO3溶液中存在水解平衡
D.常温常压下能自发进行的反应,一定都是放热反应
参考答案:D
本题解析:
试题分析:硫酸铵化学式为(NH4)2SO4,属于强酸弱碱盐,水溶液呈酸性,所以A正确;根据电荷守恒原理可知,溶液中阴离子带的负电荷总数应该等于阳离子带的正电荷,故B正确;Na2CO3属于强碱弱酸盐,水溶液呈碱性,所以滴有酚酞的溶液变红,当加入氯化钡溶液后,生成碳酸钡沉淀和氯化钠溶液,呈中性,故C正确;能否自发进行,除了和焓变有关,与熵变也有关,它们共同决定,故D错误。
考点:考查电离平衡相关知识
本题难度:一般
3、选择题 对于可逆反应: 2A(气) + B(气)  3C(气) + D(固),减少压强产生的影响的是(??)
3C(气) + D(固),减少压强产生的影响的是(??)
A.正、逆反应速率都减慢,平衡向不移动
B.正反应速率加快,逆反应速率减慢,平衡向正反应方向移动
C.逆反应速率加快,正反应速率减慢,平衡向逆反应方向移动
D.正、逆反应速率都不变,平衡向逆反应方向移动
参考答案:A
本题解析:
试题分析:降低越强,正逆反应速率都是降低,由于正反应是体积不变的可逆反应,所以平衡不移动,答案选A。
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,侧重考查学生灵活运用基础知识解决实际问题的能力,有利于培养学生的逻辑推理能力。
本题难度:简单
4、选择题 某反应A + B =" C" + D 在低温下能自发进行,在高温下不能自发进行,对该反应过程△H、△S的判断正确的是
A.△H<0 △S<0
B.△H>0 △S>0
C.△H<0 △S>0
D.△H>0 △S<0
参考答案:A
本题解析:
试题分析:反应自发进行的判断依据是△H-T△S<0分析。A、△H<0,△S<0,低温下反应自发进行,高温下不能自发进行,故A符合;B、△H>0,△S>0,高温下△H-T△S<0,反应自发进行,低温反应非自发进行,故B不符合;C、△H<0,△S>0,一定存在△H-T△S<0,在任何温度下,反应都能自发进行,故C不符合;D、△H>0,△S<0,一定存在△H-T△S>0,反应任何温度都不能自发进行,故D不符合;故选A。
考点:考查反应自发进行的判断依据和分析方法
本题难度:一般
5、填空题 某市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5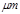 的悬浮颗粒物),其主要来源为燃煤、机动车尾气等。因此,对PM2.5、SO2、NOx等进行研究具有重要意义。
的悬浮颗粒物),其主要来源为燃煤、机动车尾气等。因此,对PM2.5、SO2、NOx等进行研究具有重要意义。
请回答下列问题:
(1)将PM2.5样本用蒸馏水处理制成待测试样。
若测得该试样所含离子的化学组分及其浓度如下表: