微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、计算题 室温下,氢氧化钠的溶解度为22 g,将多少克金属钠投入100 g水中,可获得该温度下的饱和溶液。
参考答案:将11.5 g钠投入水中可获得该温度下的饱和溶液。
本题解析:设投入100 g水中的金属钠的质量为x。
2Na+2H2O====2NaOH+H2↑
46?? 36????? 80????? 2
解法1:在一定温度下,饱和溶液中溶质的质量对应100 g溶剂的比值是一常数,建立比例关系。
质量为x的金属钠与质量为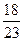 x的水反应,生成质量为
x的水反应,生成质量为
本题难度:简单
2、选择题 l mol过氧化钠与2 mol碳酸氢钠固体混合后,在密闭的容器中加热充分反应,排出气体物质后冷却,残留的固体物质是[???? ]
A. Na2CO3
B. Na2O2、Na2CO3
C. NaOH、Na2CO3
D. Na2O2、NaOH、Na2CO3
参考答案:A
本题解析:
本题难度:简单
3、选择题 将一小块金属钠投入盛少量 饱和澄清石灰水的试管里,不可能观察到的现象是
饱和澄清石灰水的试管里,不可能观察到的现象是
A.钠熔成小球并在液面上游动
B.有气体生成
C.溶液底部有银白色物质生成
D.溶液变浑浊
参考答案:C
本题解析:略
本题难度:简单
4、选择题 密闭容器中装有1mol NaHCO3和0.8mol Na2O2,加热充分反应后,容器内残留的固体是
A.0.8molNa2CO3和0.6molNaOH
B.0.5molNa2CO3和1molNaOH
C.0.8molNa2CO3和1molNaOH
D.1molNa2CO3和0.6molNaOH
参考答案:D
本题解析:1mol碳酸氢钠分解产生0.5mol二氧化碳和0.5mol水;反应中过氧化钠不足,认为二氧化碳先反应,故生成0.5mol碳酸钠和0.6molNaOH。故答案为D。
本题难度:一般
5、实验题 (12分)金属钠与水的反应是中学化学中的一个重要反应。在高中化学教材的几次改版中该实验曾出现过几种不同的演示方法,分别如下图中甲、乙、丙所示:

(1)现按图甲所示的方法,在室温时,向盛有Ca(HCO3)2溶液的水槽中,加入一小块金属钠。下列现象描述正确的是_________(填字母)。
A.钠浮在液面上,并四处游动,最后消失
B.钠熔化成一个光亮的小球
C.反应开始后,溶液由无色变红色????
D.恢复到室温时,烧杯底部有固体物质析出
(2)请补充并完成甲实验中从试剂瓶中取出钠到向水槽中投入钠的有关操作:用镊子从试剂瓶中取出一小块钠→___________________________→用镊子夹取切好的金属钠投入到盛有Ca(HCO3)2溶液的烧杯中。
(3)按图乙所示方法来收集产生的气体,需将钠包好,再放入水中。取相同质量的钠按下列几种情况收集产生的气体在相同条件下体积最大的是(???)
A.用铝箔包住钠??? B.用锡箔包住钠??? C.直接将钠投入的水中
(4)用装满水的矿泉水瓶按图丙方法进行实验,用手挤压矿泉水瓶共排出水的体积为112 mL,塞紧带有钠的塞子,反应结束后,干瘪的带塞矿泉水瓶恢复成原状,假设瓶内、瓶外均属于标准状况,则所用金属钠的质量是???????克。
参考答案:(12分)(1)A B D(3分)????
(2)用滤
本题解析:考查钠的性质及有关计算等。
(1)钠极易与水反应生成氢气和氢氧化钠,由于钠的密度小于水的,且钠的熔点很低,又因为反应放出热量,生成的氢氧化钠和碳酸氢钙反应生成碳酸钙沉淀,所以实验现象是ABD。
(2)钠保存在煤油中,而煤油是可燃性液体,所以首先要用滤纸吸干表面的煤油,然后在玻璃片上用小刀切成绿豆大小的钠粒,最后并将多余的钠放回试剂瓶中。
(3)由于铝能和氢氧化钠反应生成氢气,所以生成氢气的最多的应该是用铝箔包住的钠,答案选A。
(4)由于反应结束后,干瘪的带塞矿泉水瓶恢复成原状,这
本题难度:一般