微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 19世纪,化学家对氧化锆的化学式有争议。后经化学实验测定,锆(Zr)的相对原子质量约为91,其氯化物蒸气的密度是同温同压下H2密度的116~117倍。试推断与锆的氯化物价态相同的氧化锆的化学式为
A.ZrO
B.Zr2O
C.Zr2O3
D.ZrO2
参考答案:D
本题解析:在相同条件下,气体的密度之比是相应气体的摩尔质量之比,所以该氯化物的相对分子质量是232~234之间。由于皓元素的相对原子质量是91,所以该氯化物中氯原子的个数是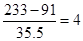 ,即皓元素的化合价是+4价,因此选项D正确,答案选D。
,即皓元素的化合价是+4价,因此选项D正确,答案选D。
本题难度:一般
2、选择题 2008年9月13日中央电视台报导了三鹿某奶粉中三聚氰胺超标使全国1200多名婴幼儿患上肾结石的“三鹿奶粉重大安全事故”。三聚氰胺是一种纯白色晶体,其化学式为C3H6N6(其相对分子质量是126)。下列关于三聚氰胺的叙述正确的是[???? ]
A.三聚氰胺的摩尔质量为126 g
B.标准状况下1mol三聚氰胺的体积约为22.4 L
C.1 mol三聚氰胺含15 NA个原子
D.63g三聚氰胺含3 g H2分子
参考答案:C
本题解析:
本题难度:简单
3、填空题 (8分)1.5 molH3PO 4的质量是??????????,含有???????????个H3PO 4分子;同温、同压下等质量的SO2和SO3气体所占的体积比为?????????,所含氧元素的质量比为???????。
参考答案:(8分) 147g ; 9.03×1023; 5:4 ; 5
本题解析:略
本题难度:一般
4、计算题 已知一个氧原子的质量为2.657×10-26kg,则多少克氧气的物质的量为1mol?(要求根据氧原子的质量进行推算)
参考答案:32g
本题解析:因为1个氧分子含2个氧原子,1 mol O2约含6.02×1023个氧分子,所以有:2.657×10-26kg×2×6.02×1023=31.99×10-3kg="32.0" g。
本题难度:简单
5、实验题 纯碱在工业上非常重要。
(1)取一定量纯碱细小粉末置于烧杯中,加入一定量的水,可以得到颗粒较大的晶体A。烧杯温度升高,理由是????????????????????????????????;
(2)从上述烧杯中得到干燥纯净的晶体A,实验程序为:??????????????;(填序号,可重复使用)
①蒸发结晶②放入干燥器③转移入过滤器中④用水洗涤2-3次⑤用乙醇洗涤⑥加热灼烧
(3)取纯净物13.92g晶体A,进行热重分析,直到质量不再改变,生成物质Z,具体数据如下:
物质
| 样品A
| T1oC下得到物质X
| T2oC下得到物质Y
| 600oC时得到物质Z
|
质量/g
| 13.92
| 11.75
| 7.45
| 6.36
通过计算确定样品A的化学式。并写出计算过程。
参考答案:(9分)(1)其化学原理为Na2CO3+ nH2O=Na2CO
本题解析:
试题分析:(1)温度升高说明发生了反应放出了热量,其化学原理为Na2CO3+nH2O=Na2CO3・nH2O,
反应物总能量高于生成物总能量,故放出热量,导致温度升高。
(2)从烧杯中得到干燥纯净的晶体A,实验程序为转移入过滤器中、用乙醇洗涤、放入干燥器。
(3)设A的化学式为Na2CO3・nH2O,加热到质量不再变化时为Na2CO3
Na2CO3・nH2O???? Na2CO3
106+18n?????????? 106
6.36
(106+18n):
本题难度:一般
|