微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列物质中属于非电解质的是( )
A.氯化氢
B.氯水
C.铜
D.二氧化碳
参考答案:D
本题解析:
本题难度:一般
2、填空题 研究化学反应原理对生产生活很有意义,请用化学反应原理的相关知识回答下列问题:
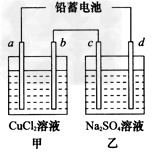
(1)如图,用铅蓄电池电解甲、乙两电解池中的溶液。已知铅蓄电池的总反应为Pb(s)+PbO2(s)+2H2SO4(aq)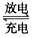 2PbSO4(s) +2H2O(l)。电解一段时间后,向c极和d极附近分别滴加酚酞试剂,c极附近溶液变红,下列说法正确的是____________(填写序号)。
2PbSO4(s) +2H2O(l)。电解一段时间后,向c极和d极附近分别滴加酚酞试剂,c极附近溶液变红,下列说法正确的是____________(填写序号)。
A.d极为阴极
B.若利用甲池精炼铜,b极应为粗铜
C.放电时铅蓄电池负极的电极反应式为PbO2(s)+4H+(aq)+ SO42-(aq)+4e-=PbSO4(s)+2H2O(l)
D.若四个电极材料均为石墨,当析出6.4gCu时,两池中共产生气体3.36L(标准状况下)
(2)某二元酸H2A在水中的电离方程式是H2A=H++ HA-:HA- H++A2-。
H++A2-。
①Na2A溶液显_______(填“酸性”“中性”或“碱性”),理由是________________(用离子方程式表示);
②已知0.1mol/L的NaHA溶液的pH=2,则0.1mol/L 的H2A溶液中氢离子的物质的量浓度可能____________(填“大于” “小于”或“等于”)0.11mol/L,理由是________________
(3)二甲醚是一种重要的清洁燃料,利用水煤气合成二甲醚的三步反应如下:
①2H2(g)+CO(g)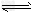 CH3OH(g) △H=-90.8kJ/mol
CH3OH(g) △H=-90.8kJ/mol
②2CH3OH(g)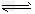 CH3OCH3(g)+H2O(g) △H=-23.5kJ/mol
CH3OCH3(g)+H2O(g) △H=-23.5kJ/mol
③CO(g)+H2O(g)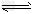 CO2(g)+H2(g) △H=-41.3kJ/mol
CO2(g)+H2(g) △H=-41.3kJ/mol
写出水煤气直接合成二甲醚同时生成CO2的热化学反应方程式:___________________。
(4)SO2是硫酸生产中的重要中间产物,也是空气污染的主要原因之一,其被氧化生成SO3的反应为2SO2(g)+O2(g)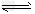 2SO3(g)。在一定温度下,将0.23molSO2和0.11molO2通入容积为1L的密闭容器中发生反应,达到平衡后得到0.12molSO3,则反应的平衡常数K=__________。若温度不变,再通入0.50molO2后重新达到平衡,则SO3的体积分数将__________(填“增大”“不变”或“减小”)。
2SO3(g)。在一定温度下,将0.23molSO2和0.11molO2通入容积为1L的密闭容器中发生反应,达到平衡后得到0.12molSO3,则反应的平衡常数K=__________。若温度不变,再通入0.50molO2后重新达到平衡,则SO3的体积分数将__________(填“增大”“不变”或“减小”)。
参考答案:(1)B
(2)①碱性;A2 -+H2O![]()
本题解析:
本题难度:一般
3、选择题 下列叙述正确的是( )
A.铜丝能导电,所以铜是电解质
B.氯化钠晶体不导电,所以氯化钠不是电解质
C.氯化氢水溶液能导电,所以氯化氢是电解质
D.SO3溶于水能导电,所以SO3是电解质
参考答案:C
本题解析:
本题难度:简单
4、选择题 下列电离方程式中,正确的是?
A.H2SO4 =H2+ +SO42-
B.NaHCO3 =Na+ +H+ +CO3-
C.Na2CO3 =2Na++CO32-
D.Ca(OH)2 = Ca 2+ +OH2一
参考答案:C
本题解析:
试题分析:A项H2SO4电离生成2个H+和1个SO42-,所以电离方程式为H2SO4 =2H+ +SO42-。B项HCO3-不能拆,所以电离方程式为NaHCO3 =Na++HCO3-。D项Ca(OH)2电离生成2个OH-和1个Ca2+,所以电离方程式为Ca(OH)2 = Ca 2+ +2OH一。答案选C。
点评:电离方程式书写正确与否首先要看是强电解质还是弱电解质,然后再看是否有不该拆的离子拆掉,该拆的离子没有拆,最后还要看物质的状态,如NaHSO4,在水溶液中应该写成NaHSO4=Na++
本题难度:一般
5、选择题 下列溶液中微粒的物质的量浓度关系正确的是[???? ]
A.0.lmol/L的NH4Cl溶液与0.05mol/L的NaOH溶液等体积混合后的溶液:c(Cl-)>c(Na+)>c(NH4+)> c(OH-)>c(H+)
B.等物质的量的NaClO、NaHCO3混合溶液中:c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3) +c(CO32-)
C.pH=2的HA溶液与pH=12的MOH溶液等体积混合:c(M+)=c(A-)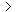 c(OH-)=c(H+)
c(OH-)=c(H+)
D.某二元弱酸的酸式盐NaHA溶液:c(OH-)+c(A2-)=c(H+)+c(H2A)
参考答案:BD
本题解析:
本题难度:一般