非金属性:P>N
参考答案:C
本题解析:
试题分析:A、电解质必须是能够自身电离出离子的化合物,氯气是单质,不是电解质,A错误;B、SO2通入硝酸钡溶液中溶液显酸性,硝酸根氧化SO2生成硫酸,进而生成硫酸钡白色沉淀,B错误;C、NaHCO3溶液与NaAlO2溶液混合产生白色沉淀,方程式为HCO3-+AlO2-+H2O=CO32-+Al(OH)3↓,这说明结合H+的能力:CO32-<AlO2-,C正确;D、非金属应该是氮元素强于磷元素,由于氮气分子中键能大,所以氮气稳定性强,D错误,答案选C。
考点:考查化学实验结论正误判断
本题难度:一般
2、选择题 下列物质中,既能导电又属于强电解质的一组物质是( )
A.熔融MgCl2、熔融NaOH
B.液氨、石灰水
C.石墨、食醋
D.稀硫酸、蔗糖
参考答案:A
本题解析:
试题分析:A.熔融MgCl2、熔融NaOH都能导电,都是强电解质,正确;B.液氨是非电解质,不能导电;石灰水能够导电,是混合物,不是电解质,错误;C.石墨、食醋都能导电,都是石墨的单质,不是电解质,食醋是混合物,错误;D.稀硫酸能够导电,是混合物,蔗糖是非电解质,错误。
考点:考查物质的分类及导电性的知识。
本题难度:一般
3、填空题 现有以下物质:①NaCl晶体 ②液态S03 ③液态的醋酸 ④汞 ⑤BaS04固体 ⑥纯蔗糖 ⑦酒精⑧熔化的KN03。 请回答下列问题(用序号)
(1)以上物质能导电的是
(2)以上物质中属于电解质的是
(3)以上物质中属于非电解质的是
(4)以上物质溶于水后形成的水溶液能导电的是
参考答案:⑴④⑧ ⑵①③⑤
本题解析:略
本题难度:一般
4、填空题 将0.1 mol的镁、铝混合物溶于100mL 2mol/L H2SO4溶液中,然后再滴加1 mol/L NaOH溶液至过量。请回答:
(1)写出与铝有关的离子方程式:
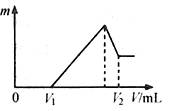
(2)若在滴加NaOH溶液过程中,沉淀质量m随加入NaOH溶液的体积V变化如图所示。当V1=160mL时,则金属粉末中n(Mg)= mol,
V2= mL。沉淀的最大质量是 g。
(3)若在滴加NaOH溶液过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积V(NaOH)= mL。
(4)若混合物仍为0.1 mol,其中Mg粉的物质的量分数为a,用100 mL 2 mol/L的硫酸溶解此混合物后,再加入450 mL 1mol/L的NaOH溶液,所得沉淀中无Al(OH)3。满足此条件的a的取值范围是: 。
参考答案:(1)2Al+6H+=2Al3++3H2↑, Al3++ 3
本题解析:略
本题难度:一般
5、选择题 下列物质中属于碱性氧化物的是 ( )
A.CO2
B.Na2O
C.Na2O2
D.FeSO4
参考答案:B
本题解析:
试题分析:能和酸反应生成盐和水的氧化物是碱性氧化物,能和碱反应生成盐和水的氧化物是酸性氧化物,所以CO2是酸性氧化物,氧化钠是碱性氧化物,过氧化钠不是碱性氧化物,硫酸亚铁是盐,答案选B。
考点:考查碱性氧化物的判断
点评:该题是基础性试题的考查,难度不大。该题的关键是明确酸性氧化物、碱性氧化物的含义以及判断依据,有利于培养学生的逻辑思维能力和创新思维能力。
本题难度:一般
|