��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� 20����30�����Eyring��Pelzer����ײ���۵Ļ����������ѧ��Ӧ�Ĺ���̬���ۣ���ѧ��Ӧ������ͨ������ײ������ɣ������ڷ�Ӧ�ﵽ������Ĺ����о���һ���������Ĺ���̬��

��1��ͼI��HI�ֽⷴӦ��HI����֮��ļ�����ײʾ��ͼ������������Ч��ײ����______��ѡ�A������B����C������
��2��ͼ����NO2��CO��Ӧ����CO2��NO�����������仯ʾ��ͼ����д��NO2��CO��Ӧ���Ȼ�ѧ����ʽ��______��
��3���±��Dz��ֻ�ѧ���ļ������ݣ�
��ѧ��
P-P
P-O
O=O
P=O
����/kJ?mol-1
198
360
498
X
��֪����ȼ����Ϊ2982kJ/mol�����ף�P4����P4O6��P4O10�ṹ����ͼ��ʾ�����ϱ���X=______��
��4��0.5mol���ף�P4����O2��ȫ��Ӧ���ɹ�̬P4O6�ų�������Ϊ______kJ��
2��ѡ���� ��NA��ʾ�����ӵ�������ֵ������˵������ȷ��
��һ�������¶��������г���3molH2(g)��1molN2(g)������Ӧ��3H2(g)+N2(g) 2NH3(g)����H=-QkJ/mol�����÷�Ӧ�ų�0��25QkJ������ʱ�������е������������2��25NA
2NH3(g)����H=-QkJ/mol�����÷�Ӧ�ų�0��25QkJ������ʱ�������е������������2��25NA
�ڳ����£�21gC3H6��C4H8�Ļ�����к��е�̼ԭ����Ϊ1��5NA
��14��2g�����ƹ����к���0��1NA�������Ʒ��ӣ�
��2gD216O�к��е�������?������?��������ΪNA
�ݱ�״���£�11��2L�ȷ��к���C-Cl������ĿΪ1��5NA
��100mL0��1mol��L-1��FeCl3��Һ�����ˮ�п��Ƶ�Fe(OH)3����0��01NA
A���٢ۢ�
B���ܢݢ�
C���٢ڢ�
D���٢�
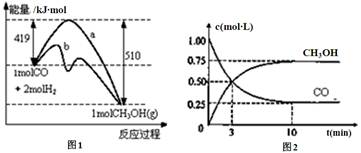
3������� ��ҵ����CO����ȼ�ϼ״���һ���¶Ⱥ��ݻ������·�����Ӧ��CO(g)+2H2(g) CH3OH(g)��ͼ1��ʾ��Ӧ�е������仯��ͼ2��ʾһ���¶��£������Ϊ1L���ܱ������м���2mol H2��һ������CO��CO��CH3OH(g)��Ũ����ʱ��仯��
CH3OH(g)��ͼ1��ʾ��Ӧ�е������仯��ͼ2��ʾһ���¶��£������Ϊ1L���ܱ������м���2mol H2��һ������CO��CO��CH3OH(g)��Ũ����ʱ��仯��
��ش��������⣺
��1���ڡ�ͼ1���У����� (�a����b��)��ʾʹ���˴�����û��ʹ�ô���ʱ���ڸ��¶Ⱥ�ѹǿ�����·�ӦCO(g)+2H2(g) CH3OH(g)�ġ�H= ��
CH3OH(g)�ġ�H= ��
��2������˵����ȷ����
A����ʼ�����CO�����ʵ���Ϊ1mol
B������CO��Ũ�ȣ�H2��ת���ʻ�����
C��������ѹǿ�㶨ʱ����Ӧ�ﵽƽ��״̬
��3���ӷ�Ӧ��ʼ������ƽ�⣬v(CO)= ���ﵽƽ��ʱ��c(H2)= �����¶���CO(g)+2H2(g)  CH3OH(g)�Ļ�ѧƽ�ⳣ��Ϊ ���ﵽƽ��������������������䣬���������ѹ��Ϊ0.5L����ƽ�� �ƶ� (�������������)��
CH3OH(g)�Ļ�ѧƽ�ⳣ��Ϊ ���ﵽƽ��������������������䣬���������ѹ��Ϊ0.5L����ƽ�� �ƶ� (�������������)��
��4����֪CH3OH(g)��3/2O2(g)��CO2(g)��2H2O(g)����H����193kJ/mol
��֪H2O(l)= H2O(g)����H����44 kJ/mol����д��32g��CH3OH(g)��ȫȼ������Һ̬ˮ���Ȼ�ѧ����ʽ ��
4��ѡ���� ��֪�����Ȼ�ѧ����ʽ��
2C��s��+O2��g���T2CO��g����H=-221kJ/mol
2H2��g��+O2��g���T2H2O��g����H=-483.6kJ/mol
�ɴ˿�֪C��s��+H2O��g���TCO��g��+H2��g����H���ڣ� ? ��
A��-131.3?kJ/mol
B��+131.3?kJ/mol
C��373.1?kJ/mol
D��-373.1?kJ/mol
5������� �����仯���������������о�����Ҫ�����á�
��1������Ԫ�����ڱ��е�λ���� ��
��2����֪�縺�Ե���ֵ��ʾԭ�ӶԵ���������������Դ�С�������Ǽ���ԭ�ӵĵ縺����ֵ��
Ԫ��
| ��
| þ
| ��
| ��
|
�縺��
| 0.9
| 1.2
| ��
| 1.8
�����ĵ縺�Ԧֵķ�Χ�� ��
�ڵ縺�Ե���ֵ��Ԫ�ؽ����ԵĹ�ϵ�� ��
������ʵ���ܱȽ�þ�����Ľ�����ǿ������ ��
a���ⶨþ�����ĵ�����ǿ��
b���ⶨ�����ʵ���Ũ�ȵ�Al2(SO4)3��MgSO4��Һ��pH
c����0.1 mol/LAlCl3��0.1 mol/L MgCl2�мӹ���NaOH��Һ
��3�����ȷ��dz��õĽ���ұ������֮һ��
��֪��4Al(s)��3O2(g)��2Al2O3(s) ��H1��-3352 kJ/mol
Mn(s)��O2(g)��MnO2(s) ��H2�� -521 kJ/mol
Al��MnO2��Ӧұ������Mn���Ȼ�ѧ����ʽ�� ��
��4��ұ��������ʱ����ʯī���缫�������Al2O3��Һ̬���ڣ�������������� ���õ����������У�����ʯī��Ҫ���ϲ��䣬��ϵ缫��Ӧ˵����ԭ���� ��
|