微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 物质的量相同的任何气体物质,一定相同的是
A.体积
B.质量
C.原子数
D.分子数
参考答案:D
本题解析:
试题分析:根据 可知,物质的量相同的任何气体物质,一定相同的是分子数,D正确,其余选项都是不一定的,答案选D。
可知,物质的量相同的任何气体物质,一定相同的是分子数,D正确,其余选项都是不一定的,答案选D。
考点:考查物质的量的有关应用
点评:该题是基础上试题的考查,学生容易错选A选项,主要是由于没有考虑到阿伏加德罗定律的使用条件,即在相同条件下,物质的量相同的任何气体物质才具有相同的体积。该题有利于培养学生严谨的逻辑思维能力。
本题难度:一般
2、选择题 设NA代表阿伏加德罗常数的数值。已知C2H4和C3H6的混合物的质量为a g,则该混合物( )
A.所含共用电子对数目为( +1)NA
+1)NA
B.所含碳氢键数目为 NA
NA
C.燃烧时消耗的O2一定是 L
L
D.所含原子总数为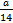 NA
NA
参考答案:B
本题解析:其最简式均为CH2,n(CH2)= ?mol,一个CH2可形成三个共用电子对,所含共用电子对数=
?mol,一个CH2可形成三个共用电子对,所含共用电子对数=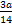 ?mol,A选项错误
?mol,A选项错误
本题难度:一般
3、选择题 NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.5.6 g铁粉在0.1mol氯气中充分燃烧,转移电子数为0.3NA
B.7.8g Na2S和Na2O2的混合物中含有的阴离子数等于0.1NA
C.12.5mL 16mol・L-1浓硫酸与足量铜反应,转移电子数为0.2NA
D.0.5mol雄黄(As4S4,结构如图)含有NA个S―S键

参考答案:B
本题解析:A. 5.6 g铁粉在0.1mol氯气中充分燃烧,铁粉有剩余,氯气反应完了,故转移电子数为0.2NA,A错误。
B. 7.8g Na2S和Na2O2的混合物为0.1mol,两种物质均只含一个阴离子,故阴离子数等于0.1NA,B正确。
C.硫酸变稀后,铜与其不再反应,故硫酸反应不完,转移电子数小于0.2NA,C错误。
D.通过观察可知,黑球表示As原子,白球表示S原子,故雄黄中不存在S―S键,D错误。
故选B
本题难度:一般
4、选择题 一定量的Fe和Fe2O3混合物投入2 mol・L-1 250 mL的HNO3溶液中,反应完全后,无固体剩余,生成1.12 L NO气体(标准状况),再向反应后溶液中加入1 mol・L-1的NaOH溶液,要使铁元素全部沉淀下来,所加NaOH溶液的体积最少是??(???????)
A.450 mL
B.500 mL
C.400 mL
D.无法确定
参考答案:A
本题解析:当完全沉淀后,恰好生成硝酸钠,实验根据原子守恒可知,硝酸钠的物质的量是(2mol/L×0.25L-1.12L÷22.4L/mol)=0.45mol,则至少需要450ml氢氧化钠溶液,答案选A。
本题难度:简单
5、计算题 (4分)某温度下的22%的NaNO3溶液 150 mL,加100 g水稀释后变为14%。求原溶液中溶质的物质的量浓度。
参考答案:(4分)解:设原溶液的质量为m
22%![]()
本题解析:略
本题难度:简单