微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (9分)现有中学化学常见的几种物质:①O2、②Mg、③CO、④WO3、⑤W、⑥CO2。请回答下列问题:
⑴①②③④四种物质中常用作还原剂的有______________ (填序号)。
⑵请将③④⑤⑥对应物质填入下列横线上,以组成一个完整的氧化还原反应方程式:???
_________+________ _______+________
_______+________
⑶随着人们环保意识的增强,许多汽车都已经装上了如图所示的尾气处理装置。在催化剂的作用下,尾气中两种主要的有毒气体反应生成两种无害气体,两种无害气体均为空气中的成分,该反应的化学方程式为____________________________________________。该反应中__________ 是氧化剂。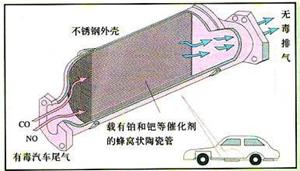
参考答案::⑴②③????? ⑵WO3? 3CO? W? 3CO2?<
本题解析:
试题分析:(1)CO是常见还原剂,Mg只能做还原剂。
(2)涉及WO3、CO、W,所以考虑是CO还原WO3,从而写出化学方程式。
(3)因为题目说到有毒气体反应生成两种无害气体,两种无害气体均为空气中的成分,无害气体为N2、CO2,从而写出化学方程式。
点评:理解氧化还原反应的概念、本质、特征。
本题难度:一般
2、填空题 下列反应中氯元素全部被氧化的是____________,全部被还原的是____________,部分被氧化的是____________,既被氧化又被还原的是____________。
A.4HCl+MnO2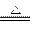 MnCl2+Cl2↑+H2O
MnCl2+Cl2↑+H2O
B.2NaCl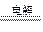 2Na+Cl2↑
2Na+Cl2↑
C.2KClO3====2KCl+3O2↑
D.Cl2+H2O====HCl+HClO
参考答案:B? C? A? D
本题解析:A项中氯元素的化合价由-1价,部分被氧化成了0价;B项中氯元素的化合价由-1价全部被氧化成了0价;C项中氯元素由+5价降为-1价,被还原,氧元素由-2价升高到0价,被氧化。D项中氯元素的化合价既有升高,也有降低,发生的是歧化反应。
本题难度:简单
3、填空题 (8分)向盛有KI溶液的试管中加入少许CCl4后滴加氯水,CCl4层变成紫色。如果继续向试管中滴加氯水,振荡,CCl4层会逐渐变浅,最后变成无色。
完成下列填空:
1)写出并配平CCl4层由紫色变成无色的化学反应方程式(如果系数是1,不用填写):

2)整个过程中的还原剂是??????????。
3)把KI换成KBr,则CCl4层变为_????????_色:继续滴加氯水,CCl4层的颜色没有变化。Cl2、HIO3、HBrO3氧化性由强到弱的顺序是???????????????。
4)加碘盐中含碘量为20mg~50mg/kg。制取加碘盐(含KIO3的食盐)1000kg,若用Kl与Cl2反应制KIO3,至少需要消耗Cl2??????L(标准状况,保留2位小数)。
参考答案:
 本题解析:略
本题解析:略
本题难度:简单
4、选择题 (宁夏固原市?2008届高三第一学期阶段性测,化学,2)某酒精厂由于管理不善,酒精滴漏到某种化学品上而酿成火灾。该化学品可能是
A.KMnO4
B.NaCl
C.(NH4)2SO4
D.CH3COOH
参考答案:A
本题解析:由于酒精是易燃物,酒精滴漏到某种化学品上而酿成火灾,则该化学品可能是强氧化性物质,即为A项中的KMnO4。
本题难度:简单
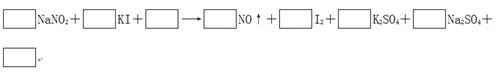
5、填空题 由于NaNO2有毒,将含该物质的废水直接排放会引起水体的严重污染,所以这种废水必须经处理后才能排放。处理方法之一的原理如下:
 ?
?
(1)请完成并配平该化学方程式。
(2)在上述反应中,若要生成50.8 g I2,则电子转移了________个。
(3)用上述反应来处理NaNO2并不是最佳方法,其原因是
________________________________________________________________________。
从环保角度来讲,要处理NaNO2,所用物质的________(填“还原性”或“氧化性”)应该比KI更______(填“强”或“弱”)。
参考答案:(1) 本题解析:
本题解析:
试题分析:(1)根据方程式可知,碘化钾中碘元素的化合价从-1价升高到0价,失去1个电子,做还原剂。亚硝酸钠中氮元素的化合价从+3价降低到+2价,得到1个电子,做氧化剂。则根据电子守恒可知氧化剂和和还原剂的物质的量之比时1:1。根据原子守恒可知,反应物中还有硫酸生成,生成物还有水生成,则反应的化学方程式是2NaNO2+2KI+2H2SO4=2NO↑+I2+K2SO4+Na2SO4+2H2O。
(2)50.8g单质碘的物质的量是50.8g÷254g/mol=0.2mol,所以转移电子的物质的量是
本题难度:一般