��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��NaBr��KI�����Һ��ͨ��������������Һ���ɲ����գ����õ��������ǣ�?��
A��NaBr��KI
B��NaBr��KCl
C��NaCl��KCl
D��NaCl��KCl�� I2
�ο��𰸣�C
�����������NaBr��KI�����Һ��ͨ������������Ӧ������嵥�ʺ͵ⵥ�ʺ��Ȼ��غ��Ȼ��ƣ�����ʱ�����嵥�����ӷ����ⵥ�����������������ʣ�µĹ���ֻ���Ȼ��غ��廯�أ���ѡC��
�����Ѷȣ���
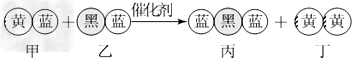
2��ѡ���� ����Ч��ת�������ɽ�����β�����ж����崦��Ϊ����Ⱦ�����壬��ͼΪ�÷�Ӧ����ʾ��ͼ(δ��ƽ)�����в�ͬ���ŵ��������ͬ��ԭ�ӡ�����˵������ȷ����
 [???? ]
[???? ]
A���÷�Ӧ����������ԭ��Ӧ
B���ͱ���ͬ��Ԫ�ػ��ϼ۲��������
C��������һ���Ƿǽ�������
D����ƽ��ס��ҡ����Ļ�ѧ��������Ϊ2
�ο��𰸣�B
���������
�����Ѷȣ���
3������� (8��)�� ��2NaOH+ Cl2 NaCl+NaClO+H2O?�� 2Na + Cl2
NaCl+NaClO+H2O?�� 2Na + Cl2 2NaCl???
2NaCl???
�� 2Fe3+ + 2I�C 2Fe2+ + I2? �� 2Fe2+ + Br2
2Fe2+ + I2? �� 2Fe2+ + Br2 2Fe3+ + 2Br�C
2Fe3+ + 2Br�C
���ĸ���ӦΪ����������̽��������ԭ��Ӧ��
��1��������ԭ��Ӧ�ı�����????????????????????????????????????????��
��2�����ڷ�Ӧ�٣���������??????????????????????????????????��
��3�����ڷ�Ӧ�ڣ�Na�Ļ��ϼ���0�۱��+1�ۣ����ϼ����ߵ�ԭ����??????????????????��
��4���ɢۡ�������Ӧ�������ƶ�Fe3+��Br2��I2��������ǿ��˳��Ϊ???????????????��
�ο��𰸣���1�����ӵ�ת�ƣ�2��Cl2��3��ʧȥ��1�����ӣ�4��Br2
���������
�����������1��������ԭ��Ӧ�ı����ǵ��ӵĵ�ʧ��ƫ�ơ���2�����ݷ���ʽ��֪��Cl2�Ļ��ϼ۽��ͣ�������������Cl2����3�������ڷ�Ӧ�ڣ�Na�Ļ��ϼ���0�۱��+1�ۣ�����ΪNaʧȥһ�����ӣ����ϼ����ߡ���4��������������������ǿ����������������ԣ����Կ����Ƴ�������Br2 ��Fe3+��I2��
��������������������ԭ��Ӧ�Ļ������⣬��Ҫ������������ԭ�Ļ������
�����Ѷȣ�һ��
4��ѡ���� �������͵ķ�Ӧ�У��������п϶��е��ʵ���(??? )
A���ֽⷴӦ
B�����ֽⷴӦ
C�����Ϸ�Ӧ
D���û���Ӧ
�ο��𰸣�D
������������⿼��������ԭ��Ӧ�ĸ���û���Ӧһ�����µĵ������ɡ�
�����Ѷȣ���
5������� �����ֻ�����Ӧ������������ԭ��Ӧ�Ĺ�ϵ��������ͼ������Т�Ϊ���Ϸ�Ӧ�����Ϊ__________��Ӧ��д���й�ˮ���ɵķ��Ϸ�Ӧ���͢��һ����ѧ����ʽ�� ______________________��д����ˮ�μӵķ��Ϸ�Ӧ���͢���һ����ѧ����ʽ __________________________������ˮΪ________����
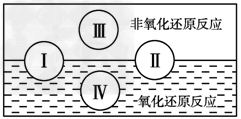
�ο��𰸣��ֽ⣻NaOH��HCl===NaCl��H2O(����������Ҳ
���������
�����Ѷȣ�һ��