微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列物质中既有离子键又有共价键的是( )
A.CaCl2
B.H2O
C.K2O
D.NaOH
2、简答题 A、B、C、D、E、F六种短周期元素的原子序数依次增大.已知A、C、F三原子的最外层共有11个电子,且这三种元素的最高价氧化物的水化物之间两两皆能反应,均生成盐和水,D元素原子的最外层电子数比次外层电子数少4个,E元素原子的次外层电子数比最外层电子数多3个.试回答:
(1)写出下列元素A的符号______,D的名称______,C的原子结构示意图______;
(2)用电子式表示B、F形成的化合物的过程:______;
(3)写出A、C两种元素最高价氧化物的水化物之间反应的离子方程式:______.
3、选择题 如表是元素周期表主族元素的一部分,已知短周期元素A最外层电子数是次外层的三倍.下列关于这四种元素说法正确的是( )
| | | | | A
B
C
D
A.气态氢化物的稳定性:A<D
B.原子半径:B<C<A<D
C.A与B组成的两种化合物均只由离子键构成
D.B、C、D三种元素的最高价氧化物对应水化物间可两两反应
4、填空题 我国已研制出一种稀土制冷材料,其主要成分是LaCaMnO。
(1)锰原子的基态价层电子排布式为________。
(2)S与O为同主族元素,其中电负性较大的是________;H2S分子中S原子杂化轨道类型为________;试从结构角度解释H2SO4的酸性大于H2SO3的酸性:____________。
(3)Ca在空气中点燃生成CaO和少量Ca2N2。
①Ca2N2和水反应可以生成NH2―NH2,NH2―NH2能否作配体?________(填“能”或“否”)。
②CaO晶体与NaCl晶体一样,为面心立方最密堆积,则一个CaO晶胞中含有Ca2+数为________;欲比较CaO与NaCl的晶格能大小,需考虑的数据是________。
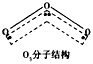
5、填空题 臭氧层能吸收紫外线,保护人类赖以生存的空间。O3分子的结构如图所示,键角为116.5°三个原子以一个O原子为中心,与另外两个O原子分别构成一个非极性共价键;中间O原子提供2个电子,旁边两个O原子各提供1 个电子,构成一个特殊的化学键(虚线内部分)--三个0 原子均等地享有这4个电子。
请回答
(1)题中非极性共价键是______键,特殊的化学键是______键。
(2)臭氧与氧气的关系是_________
(3)下列物质的分子与O3分子的结构最相似的是______
A.H2O B.CO2 C.SO2 D.BeCl2
(4)分子中某一原子没有跟其他原子共用的电子对叫孤电子对,那么O3分子中有______对孤电子对。
|