微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (10分)能源问题是人类社会面临的重大课题,甲醇是未来重要的能源物质之一。
(1)合成甲醇的反应为:CO(g)+2H2(g) CH3OH(g)△H;右图表示某次合成实验过程中甲醇的体积分数φ(CH3OH)与反应温度的关系曲线,则该反应的△H???????
CH3OH(g)△H;右图表示某次合成实验过程中甲醇的体积分数φ(CH3OH)与反应温度的关系曲线,则该反应的△H???????
??????????0(填“>、<或= ”)

(2)若在230℃时,平衡常数K=1。若其它条件不变,将温度升高到500℃时,达到平衡时,K???1 (填“>、<或= ”)
(3)在某温度下,向一个容积不变的密闭容器中通入2.5mol CO和7.5mol H2,达到平衡时CO的转化率为90%,此时容器内的压强为开始时的?????倍。
(4)利用甲醇燃料电池设计如右图所示的装置:则该装置中Cu极为??????????极。
①写出b极的电极反应式????????????????????。
②当铜片的质量变化为12.8 g时:a极上消耗的O2在标准状况下的体积为??????L。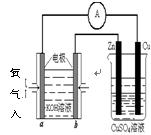
参考答案:
(1)<(2分)
(2)<(1分)
本题解析:略
本题难度:简单
2、实验题 (14分)该图是某化学课外活动小组设计的乙醇与氢卤酸反应的实验装置图。在烧瓶A中放一些新制的无水硫酸铜粉末,并加入约20 mL无水乙醇;锥形瓶B中盛放浓盐酸;分液漏斗C和广口瓶D中分别盛浓硫酸;干燥管F中填满碱石灰;烧杯作水浴器。当打开分液漏斗的活塞后,由于浓硫酸流入B中,则D中导管口有气泡产生。此时水浴加热,发生化学反应。过几分钟,无水硫酸铜粉末由无色变为蓝色,生成的气体从F顶端逸出。(已知一氯乙烷沸点:12.3℃)试回答:

(1)B逸出的主要气体名称__________;
(2)D瓶的作用是___________________;
(3)E管的作用是_____________________;
(4)F管口点燃的气体分子式__________________
(5)A瓶中无水硫酸铜粉末变蓝的原因是______________________________;
(6)A中发生反应的化学方程式:________________________________________________
参考答案:(1)氯化氢(2)吸收氯化氢气体中混有的水蒸气(3)冷凝乙醇
本题解析:略
本题难度:简单
3、选择题 下列说法错误的是(????)
A.乙醇和乙酸都是常用调味品的主要成分
B.乙醇和乙酸的沸点和熔点都比C2H6、C2H4的沸点、熔点高
C.乙酸和乙醇都能发生氧化反应
D.乙醇和乙酸之间能发生酯化反应,酯化反应和皂化反应互为逆反应
参考答案:D
本题解析:
试题分析:A.乙醇是料酒的主要成分;而乙酸则是食醋的主要成分。因此它们都是常用调味品的主要成分。正确。B.乙醇和乙酸的相对分子质量比C2H6、C2H4大。相对分子质量越大,分子间的作用力就越强,则物质的熔沸点就越高。因此乙醇和乙酸的沸点和熔点都比C2H6、C2H4的沸点、熔点高。正确。C.乙酸和乙醇都能发生燃烧反应而被氧化。除此之外,乙醇还能被催化氧化剂被酸性高锰酸钾hi重铬酸钾溶液氧化。正确。D.乙醇和乙酸之间能在浓硫酸作催化剂条件下发生酯化反应,酯化反应和酯的水解反应互为逆反应,但是皂化反应是
本题难度:简单
4、选择题 下列化合物中,在常温常压下以液态形式存在的是 [???? ]
A.甲醇
B.乙炔
C.丙烯
D.丁烷
参考答案:A
本题解析:
本题难度:简单
5、选择题 乙醇作为燃料的优点是:
①燃烧时发生氧化反应 ??②充分燃烧的产物不污染环境
③乙醇是一种可再生能源 ④燃烧时放出大量热量
A.①②③
B.①②④
C.①③④
D.②③④
参考答案:D
本题解析:其它燃料燃烧也会发生氧化反应,所以①不是乙醇作为燃料的优点,那么乙醇燃烧的产物不污染环境,是可再生能源,燃烧使放出大量热等,都是乙醇燃料的优点,故选D
本题难度:简单