��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �ס��ҡ�����������Ԫ��λ��ͬһ�����ڣ�ԭ�������������ӡ������жϴ������
A��ԭ�Ӱ뾶�������ң���
B�����ס��ҡ��������ĵ����ڳ����¾�Ϊ��̬����˵�����ȼ���1��Ԫ���γɵĵ����۵���ܸܺߡ�
C�����ס��ҡ������ǽ�����������������ԣ��ף��ң���
D�����ҵ���ۺ�����Ϊǿ�ᣬ����ǻ��÷ǽ���Ԫ��
�ο��𰸣�C
���������
�����Ѷȣ�һ��
2������� �����������ʵ���Ҫ���������ʵĽṹ����ش��������⣺
��1����֪A��BΪ��������Ԫ�أ���ԭ�ӵĵ�һ�����ĵ��������±���ʾ��
������/kJ��mol��1
| I1
| I2
| I3
| I4
|
A
| 578
| 1817
| 2745
| 11578
|
B
| 738
| 1451
| 7733
| 10540
Aͨ���� ��?�ۣ�A�ĵ縺��???��??B�ĵ縺��(�����������������)��
��2����֪������Ϊ300 nm�������Ĺ��ӣ����ӵ���������Ƶ�ʵĹ�ϵΪE��hv��ʽ��h��6.63��10��34J��s����IJ���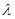 ����Ƶ��v�Ĺ�ϵΪ ����Ƶ��v�Ĺ�ϵΪ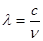 �����й���c=3��108m��s-1�������±��йص����ʷ�������Ҫ��ѧ������Ϣ����Ϊ300 nm�������Ĺ��������е���������������kJ��mol��1��˵�����峤ʱ������������Ƥ���Ƿ�����˺���ԭ��????���������������� �����й���c=3��108m��s-1�������±��йص����ʷ�������Ҫ��ѧ������Ϣ����Ϊ300 nm�������Ĺ��������е���������������kJ��mol��1��˵�����峤ʱ������������Ƥ���Ƿ�����˺���ԭ��????����������������
��??????������������������??����δ˵��ԭ���֣�
���ۼ�
| C��C
| C��N
| C��S
| ����/kJ��mol��1
| 347
| 305
| 259
��3����ѧ��ͨ��X����̽����KCl��MgO��CaO��TiN�ľ���ṹ��NaCl�ľ���ṹ���ơ��±���3�����Ӿ���ľ��������ݣ�
���Ӿ���
| NaCl
| KCl
| CaO
| ������/kJ��mol��1
| 786
| 715
| 3401
���Ӽ���ǿ�����������Ӿ���ľ�������������KCl��CaO��TiN 3�����Ӿ����۵�Ӹߵ��͵�˳����??��??��MgO������һ��Mg2����Χ�������ڽ��ҵȾ����Mg2����?��?����
��4���о����ʴ��Ա��������������Ӻ�δ�ɶԵ���Խ�࣬�����Խ�ż�¼����Խ�á�������������V2O5��CrO2�У��ʺ���¼�����ŷ�ԭ�ϵ���???????��?????��
��5�� [Cu(NH3)4]SO4�д��ڵĻ�ѧ��������????????????????????������ţ���
A�����ۼ�?? B�����??? C�����Ӽ�??? D����λ��??? E�����Ӽ�������???
NH3���ӵĿռ乹��Ϊ�������������������������������������ӣ�����ԡ��Ǽ��ԡ���
�ο��𰸣���1����3��1�֣�������1�֣���2��399��1�֣����������
���������
�����Ѷȣ�һ��
3������� ����A��B��C��D��E��F����Ԫ�أ�Aԭ�Ӻ���ֻ��һ�����ӣ�B�����������Ǵ�����������2����CԪ�ص����������ӵ�3d�ܼ�Ϊ������� Eԭ�ӵ�M���N��ֱ��Dԭ�ӵ�M���N���5�����ӣ�Fԭ�ӵ�N��ֻ��һ�����ӣ���M��Ϊȫ������
��1��д��B�Ļ�̬ԭ�ӵļ۵��ӹ����ʾʽ???????????????????????
��2��C��Ԫ�ط���?????�����̬ԭ�ӵĵ����Ų�ʽΪ??????????????????????
��3����E��C�ܷ�Ӧ�������ӻ�����CE3,��D��ԭ�ӽṹʾ��ͼΪ????????????????????��A��B��ԭ�Ӹ�����Ϊ1:1��ɵ���Է�������Ϊ78�ķ�������E�ĵ��ʷ�Ӧ�Ļ�ѧ����ʽΪ???????????????????????????????
��4����Ԫ��F������������μ��백ˮ��������д���ù����漰��Ӧ�����ӷ���ʽ��
?????????????????????????????????????????????????????????????????
�ο��𰸣���1�� ��������� ���������
�����Ѷȣ���
4������� (6��)����As�ķ�Ӧ�У���Ӧ�����������У�AsH3��H2SO4��KBrO3��K2SO4��H3AsO4��H2 O��һ��δ֪����X�� O��һ��δ֪����X��
����֪KBrO3�ڷ�Ӧ�еõ����ӣ���÷�Ӧ�Ļ�ԭ����_____________��
����֪0��2mol KBrO3�ڷ�Ӧ�еõ�1mol��������X����X�Ļ�ѧʽΪ_______________________________________________��
�۸���������Ӧ����֪________________��(�����)
A�������ԣ�KBrO3>H3AsO4
B�������ԣ�H3AsO4>KBrO3
C����ԭ�ԣ�AsH3>X
D����ԭ�ԣ�X>AsH3
���ڸ÷�Ӧ�У��������뻹 ԭ�������ʵ���֮��Ϊ_______________�� ԭ�������ʵ���֮��Ϊ_______________��
�ο��𰸣���AsH3��1�֣�?��Br2��1�֣�???��A��C��ȫ��2��
���������
�����Ѷȣ�һ��
5������� ��������s�ܼ�p�ܼ���ԭ�ӹ��ͼ���Իش����⣺ s���ӵ�ԭ�ӹ����?????�Σ�ÿ��s�ܼ���?????��ԭ�ӹ����p���ӵ�ԭ�ӹ����?????�Σ�ÿ��p�ܼ���?????��ԭ�ӹ����
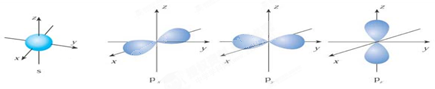
��д������Ԫ�ػ�̬ԭ�ӵĵ����Ų�ʽ��
��1��Ca???????????????????????????��
��2��Kr???????????????????????????��
��3��Co???????????????????????????��
��4��Ge???????????????????????????��
�ο��𰸣�(16��)��.���� �� 1 �� �Ĵ� �� 3?��
��.
���������
�����Ѷȣ�һ��
|
|
|
��վ�ͷ�QQ: 960335752 - 14613519 - 791315772