微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、推断题 有A、B、C、D、E五种元素,原子序数依次增大,位于不同的三个短周期,其中B与D为同一主族元素,它们可形成化合物DB2、DB3,在同周期元素中,C的金属性最强,E的非金属性最强;请回答:
(1)写出A、E三种元素的名称:A____________,E_____________。
(2)A、B形成的原子个数比为1∶1的化合物的电子式为__________________,该化合物与DB2化合生成一种强酸的化学方程式为:__________________________。
(3)已知在一定条件下1mol DB2完全转化为气态DB3,放出98.3 kJ的热量。该反应的热化学方程式是
_____________________________,工业上进行这一反应的设备是_____________,反应的适宜条件为
________________________。
(4)用铂作电极电解由C、E形成化合物的饱和溶液时,检验阳极产物的实验方法为________________________________________;电解一段时间后,将阳极产物和阴极溶液混合,反应的离子方程式是
_____________________________。工业实际中常采用阳离子交换膜电解槽进行电解,若某一电极由碳钢网制成,则该电极为电解槽的___________(填“阴”或“阳”,下同)极,精制的由C、E形成的化合物的饱和溶液进入_________极室。
参考答案:(1)氢;氯
(2)![]() 本题解析:
本题解析:
本题难度:一般
2、填空题 A、B、C、D、E都是元素周期表中前20号元素,原子序数依次增大,B、C、D同周期,A、D同主族,E和其它元素既不在同周期也不在同主族,D的最高价氧化物的水化物为强酸,且B、C、D的最高价氧化物的水化物两两混合均能发生反应生成盐和水。根据以上信息,回答下列问题:
(1)A和D氢化物中,沸点较低的是____________(选填A或D);A离子和B离子中,半径较小的是____________(填离子符号)。
(2)元素C在元素周期表中的位置是____________________。
(3)写出C的最高价氧化物的水化物分别与B、D的最高价氧化物的水化物反应的离子方程式_________________________、________________________。
(4)下图表示由上述五种元素中的两种元素所形成的离子化合物的晶胞(晶胞是在晶体中具有代表性的最小重复单元)。阳离子(用“・ ”表示)位于该正方体的顶点和面心;阴离子(用“○”表示)均位于小正方体中心。该化合物的化学式可能是___________、_____________。
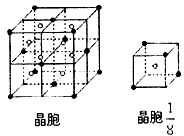
参考答案:(1)D;Na+?
(2)第三周期、ⅢA族
本题解析:
本题难度:困难
3、选择题 已知80Hg是第六周期第ⅡB族元素,第七周期ⅡB族元素的原子序数是
A.112
B.98
C.88
D.82
参考答案:A
本题解析:
本题难度:简单
4、选择题 下列叙述中能说明A的金属性比B强的是( )
A.A原子的最外层电子数比B原子的最外层电子数少
B.A最高价氧化物的水化物的碱性比B最高价氧化物的水化物的碱性强
C.1molA从酸中置换出的H2比1molB从酸中置换的H2多
D.A的阳离子的氧化性比B阳离子的氧化性强
参考答案:A.比较金属性的强弱不能从最外层电子的多少来判断,例如Ca的
本题解析:
本题难度:一般
5、选择题 如图所示是元素周期表前六周期的一部分,关于元素X、Y、Z的叙述正确的是( )
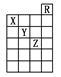
①X的气态氢化物与Y的最高价氧化物对应的水化物能发生反应生成盐
②X、Y、Z的气态氢化物的水溶液的酸性X<Y<Z
③Z的单质在常温下是液体,可与铁粉反应
④Z的原子序数比Y大19
⑤Z所在的周期中含有32种元素
A.只有③
B.①④
C.①②③④
D.①②③④⑤
参考答案:C
本题解析:试题分析:元素X、Y、Z分别为N、S和Br,X的气态氢化物为NH3,Y的最高价氧化物对应的水化物为H2SO4,生成的盐为硫酸铵,①正确;NH3是碱性气体,H2S水溶液是弱酸,HBr水溶液是强酸,②正确;HBr常温下是液体,与铁粉反应生成FeBr3, ③正确;Z、Y原子序数分别为35和16,④正确;Z为第四周期,含有18中元素,⑤错误。
考点:元素周期表及其规律
点评:元素周期表及其规律是高考必考知识点,考生应理解掌握元素周期律,并灵活运用。
本题难度:困难