��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �ϳɰ�����H2����ú��ˮ��Ӧ�Ƶã�����һ����ӦΪ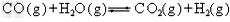 ������Ӧ�Ƿ��ȷ�Ӧ���������CO��ת���ʿɲ��õķ����У��ټ�Сѹǿ���ڽ����¶ȣ�������ˮ������Ũ�ȣ�������CO��Ũ�ȣ���ʹ�ô�����������ȷ������� [???? ]
������Ӧ�Ƿ��ȷ�Ӧ���������CO��ת���ʿɲ��õķ����У��ټ�Сѹǿ���ڽ����¶ȣ�������ˮ������Ũ�ȣ�������CO��Ũ�ȣ���ʹ�ô�����������ȷ������� [???? ]
A���ڢ�????
B���ڢ�?????
C���٢�???
D��ֻ�Т�
�ο��𰸣�B
���������
�����Ѷȣ�һ��
2��ѡ���� ������ƽ��2CrO42-����ɫ��+2H+?Cr2O72-���Ⱥ�ɫ��+H2O�У���Һ���ڻƺͳȺ�ɫ֮�䣬����������Һ�ijȺ�ɫ����Ҫ����Һ�м��루������
A��H+
B��OH-
C��K+
D��H2O
�ο��𰸣�A������Һ�м��������ӣ�������Ũ������ƽ��������Ӧ�����ƶ�
���������
�����Ѷȣ���
3��ѡ���� ��һ���¶��£�������������ֱ�ͨ����ʼ�����ͬ���ܱ�������͢��У�ʹ�䷢����Ӧ��t0ʱ�������дﵽ��ѧƽ�⣬X��Y��Z�����ʵ����ı仯��ͼ��ʾ���������й��ƶ���ȷ����?��������
A���÷�Ӧ�Ļ�ѧ����ʽΪ3X+2Y?2Z
B�����������о��ﵽƽ��ʱ�������������V����V������������ﵽƽ������ʱ�����t0
C�����������о��ﵽƽ��ʱ����������Z�����ʵ���������ͬ����YΪ��̬��Һ̬
D������ƽ��������������¶�ʱ���������˵��Z�����ķ�ӦΪ���ȷ�Ӧ
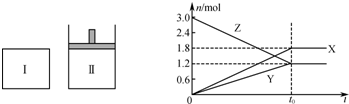
�ο��𰸣�A������XYZ���ʵ����ı仯ͼ�������Z�Ƿ�Ӧ�XY������
���������
�����Ѷȣ���
4������� �����ж�����Ӧ����Fe��s��+CO2��g���TFeO��s��+CO��g����ƽ�ⳣ��ΪK1��
��Fe��s��+H2O��g���TFeO��s��+H2��g����ƽ�ⳣ��ΪK2������ڲ�ͬ�¶��£�K1��K2ֵ���£�
| �¶�/�� | K1 | K2
500
1.00
3.15
700
1.50
2.25
900
2.50
1.50
��1����500��ʱ���з�Ӧ�٣�CO2��ʼŨ��Ϊ2mol/L��CO2��ת����Ϊ______��
��2����һ�����Ϊ10L���ܱ������У�����������Fe��FeO��ĩ��Ȼ��
���ٳ���CO2��H2O��g����1mol������һ�����¶ȣ����϶�����Ӧͬʱ�ﵽƽ�⣮��______��c(CO)
c(H2)
��ֵ���
���ٳ���CO22mol��H2?4mol��������900�棬���϶�����Ӧ�ﵽƽ�����ƽ��ʱ�������������______��
�ο��𰸣���1����CO2��Ũ�ȱ仯��Ϊcmol/L���ɷ���ʽ��֪CO��
���������
�����Ѷȣ�һ��
5��ѡ���� ���и�������ʾ��ͼ��һ�µ���
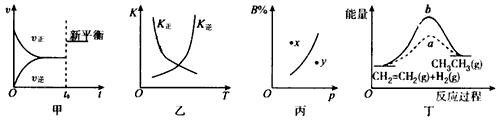 [???? ] [???? ]
A����ͼ��ʾһ�����淴Ӧ�ﵽƽ��״̬�������ʹ���˴���
B����ͼ�����߱�ʾ��Ӧ2SO2(g)+O2(g)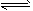 2SO3(g) ��H<0�������淴Ӧ��ƽ�ⳣ��K���¶ȵı仯 2SO3(g) ��H<0�������淴Ӧ��ƽ�ⳣ��K���¶ȵı仯
C���Է�ӦaA(g)+bB(g)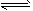 cC(g)��˵����ͼx���ʾ����Ӧ��ѹǿ�����¸÷�Ӧ����������Ӧ������� cC(g)��˵����ͼx���ʾ����Ӧ��ѹǿ�����¸÷�Ӧ����������Ӧ�������
D����ͼ��a��b���߷ֱ��ʾ��ӦCH2=CH2(g)��CH3CH3(g) ��H<0��ʹ�ú�δʹ�ô���ʱ����Ӧ�����е������仯
�ο��𰸣�D
���������
�����Ѷȣ�һ��
|
|