微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 【化学―选修2:化学与技术】(15分)
石膏转化为硫酸钾和CaCl2的工艺流程如下:

(1)CO2是一种很重要的副产品,工业上获得CO2的途径是 ?(用化学方程式表示)。
(2)转化Ⅰ中发生反应的离子方程式为 。过滤Ⅰ得到的滤液是 ,检验滤液中含有CO的方法是_________________________________。
(3)转化Ⅱ中发生反应的化学方程式为 ,转化Ⅱ中可获得K2SO4的原因是__________________________________________________。
(4)上述工艺流程中体现绿色化学理念的是______________________________________。
(5)氯化钙结晶水合物是目前常用的无机储热材料,选择的依据是 。
a.熔点较低(29 ℃熔化)????????b.能制冷
c.无毒???????????????????????d.能导电
参考答案:(1)CaCO3 本题解析:(1)工业生产生石灰的同时会产生大量的CO2气体,这是工业上获得CO2的主要来源。
本题解析:(1)工业生产生石灰的同时会产生大量的CO2气体,这是工业上获得CO2的主要来源。
(2)碳酸钙的溶解度大于硫酸钙的,所以硫酸钙可以和碳酸盐反应生成碳酸钙。因此硫酸钙和碳酸铵反应生成碳酸钙和硫酸铵,即滤液中的主要成分是硫酸铵。碳酸盐和盐酸可以反应生成能使澄清石灰水变混浊的气体CO2,据此可以鉴别。
(3)当硫酸铵和氯化钾混合后,由于KCl、(NH4)2SO4、K2SO4、NH4Cl四种物质的溶解度受温度的影响不同,所以可以通过控制溶液的温度得到硫酸钾固体。
(4)根据转化特点可知,氨气在
本题难度:一般
2、填空题 (12分)、高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺如下:
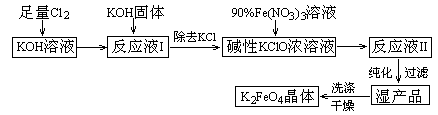
已知:①? 2KOH + Cl2 → KCl + KClO + H2O(条件:温度较低)
②? 6KOH + 3Cl2 → 5KCl + KClO3 + 3H2O(条件:温度较高)
③? 2Fe(NO3)3 + 2KClO + 10KOH → 2K2FeO4 + 6KNO3 + 3KCl + 5H2O
回答下列问题:
⑴该生产工艺应在???__???(填“温度较高”或“温度较低”)的情况下进行;
⑵写出工业上制取Cl2的化学方程式????????__??????????;
⑶配制KOH溶液时,是在每100 mL水中溶解61.6 g KOH固体(该溶液的密度为1.47 g/mL),它的物质的量浓度为?????__?????;
⑷在“反应液I”中加KOH固体的目的是???????????__?????????????:
A.与“反应液I”中过量的Cl2继续反应,生成更多的KClO
B.KOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供反应物
D.使副产物KClO3转化为 KClO
⑸从“反应液II”中分离出K2FeO4后,会有副产品???_?????(写化学式),它们都是重要的化工产品,具体说出其中一种物质的用途???_????。
参考答案:(1)温度较低(2分)
(2)2NaCl + 2H2O
本题解析:⑴根据工艺流程图,反应液I除去KCl主要是KClO溶液,氯气在较低温度下和KOH反应才得到KClO,所以,应在较低温度下进行。
⑵工业上制取Cl2是电解饱和的食盐水,化学方程式:2NaCl + 2H2O 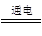 ?2NaOH + H2↑ + Cl2↑
?2NaOH + H2↑ + Cl2↑
⑶所配KOH溶液的物质的量浓度为:n(KOH )="61
本题难度:一般
3、选择题 下列冶炼金属的原理中,属于热还原法的是
A.2Ag2O 4Ag+O2↑
4Ag+O2↑
B.Fe2O3+3CO 2Fe+3CO2↑
2Fe+3CO2↑
C.Fe+CuSO4=FeSO4+Cu
D.MgC12 Mg+C12↑
Mg+C12↑
参考答案:B
本题解析:A是加热分解,C是活泼金属的置换,D是电解法,所以正确的答案选B。
本题难度:一般
4、填空题 (8分)海水的综合利用,对于人类的生产生活有重要的意义。
(1)海水淡化沿海缺水地区获取淡水的方法之一,列举出海水淡化的两种方法?????????、???????????。
(2)氯碱工业离子交换膜法生产中,透过离子交换膜的离子为????????,氢氧化钠产生于????????(填‘“阳极”或“阴极”)。
(3)氯化钠为工业制纯碱的主要原料,制碱反应过程中法中析出NaHCO3的原因是?????????????????????????????????????????????????;侯氏制碱法与索尔维制碱法相比除提高食盐利用率、无氯化钙生成的优势外还有????????????????????????、???????????????????从而综合利用原料、降低成本、减少环境污染。
参考答案:(8分)(1)蒸馏法(1分)?电渗析法(1分)?(2)Na+
本题解析:(1)海水中含有大量的Na+、Mg2+等,故海水淡化的常用方法是蒸馏法和电渗析法。
(2)氯碱工业的生成物是氯气、氢气和氢氧化钠,其中氢氧化钠在阴极生成,所以透过离子交换膜的离子是Na+。
(3)由于饱和额食盐水中溶解了大量的氨气,因而可以吸收大量的二氧化碳生成碳酸氢钠,而NaHCO3溶解度相对较小,从而饱和后析出。侯氏制碱法需要氨气,故可以与合成氨联合生产,在生成碳酸氢钠的同时还有氯化铵生成。
本题难度:一般
5、选择题 与普通玻璃具有相同组成的是( )
A.钢化玻璃
B.光学仪器玻璃
C.石英玻璃
D.有色玻璃
参考答案:A?
本题解析:钢化玻璃是把普通玻璃放入电炉中加热变软后急剧冷却后得到的,它和普通玻璃的成分相同。光学玻璃中加有PbO,有色玻璃中则加入了金属氧化物
本题难度:简单