微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 向一体积不变的密闭容器中加入2mol A、0.6mol C和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如图一所示。图二为t2时刻后改变反应条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件。已知t3~t?4阶段为使用催化剂;图一中t0~t1阶段c(B)未画出。

下列说法不正确的是(??)
A.此温度下该反应的化学方程式2A(g)+B(g) 2C(g)
2C(g)
B.t4~t5阶段改变的条件为减小压强
C.B的起始物质的量为1.0mol
D.在相同条件下,若起始时容器中加入a mol A、bmol B和cmol C,要达到t1时刻同样的平衡,a、b、c要满足的条件为a+ =2.4 和 b+
=2.4 和 b+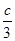 =1.2
=1.2
参考答案:A
本题解析:本题以图像的形式考查影响化学反应速率以及化学平衡移动的因素。图二是在四种不同情况下影响化学的平衡,而影响平衡的因素有:浓度、温度、压强、催化剂,t3~t4和t4~t5这两段平衡是不移动的,则只能是压强和催化剂影响的,因此应该推断该反应为等体积变化的反应。再结合图一可知,A的变化为0.2mol/L,C的变化量为0.3mol/L,由规律知,化学反应的速率之比等于化学方程式前的计量系数比,可写出该反应的方程式为2A(g)+B(g) 本题难度:一般
本题难度:一般
2、选择题 下列描述违背化学原理的是( )
A.“冰,水为之,而寒于水”,说明相同质量的水和冰,水的能量高
B.可逆反应A(g)+3B(g)?2C(g)达平衡后,增大压强,正速率增大,逆速率减小
C.SO2的催化氧化生成SO3,是一个放热的反应,升高温度,反应速率加快
D.电解熔融NaCl时,阴极的电极反应式为:Na++e-=Na
参考答案:A.液态水的能量比固态水的能量高,水变成冰要放出热量,故A正
本题解析:
本题难度:简单
3、简答题 在一可变容积的密闭容器中进行反应:C(s)+H2O(g)=CO(g)+H2(g),下列条件能使反应速率增大的是( )
A.增加C的量
B.将容器的体积缩小一半
C.保持体积不变,充入N2,使体系的压强增大
D.保持压强不变,充入N2,使容器的体积变大
参考答案:A、因该反应中只有C为纯固体,则增加C的量对化学反应速率无影
本题解析:
本题难度:一般
4、填空题 (1)把镁条投入盛有盐酸的敞口容器中,产生氢气速率变化如图所示。在反应过程中导致速率变化的因素有___________
①H+的浓度
②镁条的表面积
③溶液的温度
④Cl-的浓度

?(2)影响速率的有关因素有:物质本身的性质、浓度、温度、催化剂等方面,依据影响速率的有关因素分析下列问题:
①Mg和Fe均可以与O2反应, Mg在空气中可以点燃, Fe在空气中不能点燃,是由于_________的影响;
②Fe在空气中加热不能燃烧,但在纯氧中可以,是由于_________的影响;
参考答案:(1)①③
(2)物质本身的性质;氧气浓度
本题解析:
本题难度:一般
5、选择题 对于反应2SO2(g)+O2(g)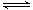 2SO3(g),能增大正反应速率的措施是(????)
2SO3(g),能增大正反应速率的措施是(????)
A.移去部分SO3
B.增大容器的体积
C.通入大量O2
D.升高体系温度
参考答案:C
本题解析:考查外界条件对反应速率的影响。降低浓度或降低压强,反应速率降低。增大浓度或升高温度,反应速率增大,因此答案选CD。
本题难度:简单