微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列图示与对应的叙述相符的是( )

图甲 图乙 图丙 图丁
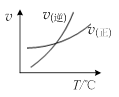
A.由图甲表示的反应速率随温度变化的关系可知该反应的ΔH>0
B.图乙表示pH相同的 盐酸与醋酸中分别加入水后溶液pH的变化,其中曲线a对应的是醋酸
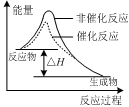
C.图丙表示该反应为放热反应,且催化剂能改变反应的焓变
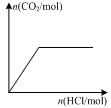
D.图丁表示向Na2CO3溶液中逐滴滴加稀盐酸,生成CO2与所加盐酸物质的量的关系
2、填空题 某二元弱酸(简写成H2A)溶液,按下式发生一级和二级电离:H2A?H++HA-,HA-?H++A2-,已知同浓度时电离程度H2A远大于HA-.设有下列四种溶液:
①0.01mol/LH2A溶液
②0.01mol/LNaHA溶液中
③0.02mol/LHCl与0.04mol/LNaHA等体积混合
④0.02mol/LNaOH与0.02mol/LNaHA等体积混合
(1)写出溶液③中HCl和NaHA反应的离子方程式______;
(2)四种溶液中c(H+)从大到小的顺序是______;
(3)四种溶液中c(A2-)最大的是______,最小的是______.
3、填空题 已知HA是一种弱酸。请回答下列问题:
(1)现有一种含有HA和其钠盐NaA的溶液。
①组成该溶液的微观粒子有??????????;
②若向该溶液中加入少量盐酸时,发生反应的离子方程式是?????????????????????;
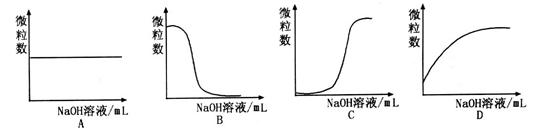
③若向该溶液中逐滴加入NaOH溶液时,下列图像能表示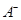 离子数目变化趋势的是????????(填字母)。
离子数目变化趋势的是????????(填字母)。
(2)现将1体积0.04mol 溶液和1体积0.02mol
溶液和1体积0.02mol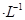 NaOH溶液混合,得到2体积混合溶液。
NaOH溶液混合,得到2体积混合溶液。
①若该混合液显碱性,则其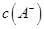 ???????????0.01 mol
???????????0.01 mol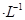 (填“<”、“=”或“>”);
(填“<”、“=”或“>”);
②若该混合液显酸性,则溶液中所有离子的浓度由大到小的顺序是??????????。
4、选择题 常温下,0.1 mol/L某一元酸(HA)溶液中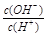 =1×10-8,下列叙述正确的是(? )
=1×10-8,下列叙述正确的是(? )
A.溶液中水电离出的c(H+)=10-10 mol/L??
B.溶液中c(H+)+c(A-)=0.1 mol/L
C.溶液中加入一定量CH3COONa晶体或加水稀释,溶液的c(OH-)均增大
D.与0.05mol/LNaOH溶液等体积混合后所得溶液中离子浓度大小关系为c(A-)>c(Na+)>c(OH-)>c(H+)
5、选择题 下列事实中,能说明HNO2是弱电解质的是
A.用HNO2溶液做导电性实验,灯泡较暗
B.HNO2是共价化合物
C.HNO2溶液不与NaCl反应
D.室温下,0.1mol・L-1 HNO2溶液的pH为2.15