��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��ͼ��ʾ����ԲȦ�ཻ�IJ��ֱ�ʾԲȦ�ڵ�����������ķ�Ӧ����֪�Ƽ�������������ʵ�����Ϊ0.1mol��ˮ������Ϊ100g������˵����ȷ���ǣ�������
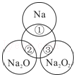
A��Na2O2������������Ŀ֮��Ϊ1��1
B����Ӧ�ٵ����ӷ���ʽΪ��Na+2H2O=Na++2OH��+H2��
C����Ӧ������ܲ���0.05mol O2
D���١��ڡ��۳�ַ�Ӧ��������Һ�����������Ӵ�С���٣��ڣ���
�ο��𰸣�C��
���������
���������A��������������������O2 2������������������Ŀ֮��Ϊ1��2����A����
B����Ӧ�ٵ����ӷ���ʽΪ��2Na+2H2O=2Na++2OH��+H2������B����
C����Ӧ����ʽΪ��2Na2O2+2H2O=4NaOH+O2����
2mol???????????? 1mol
0.1mol?????????? 0.05mol
���ݷ���ʽ֪��������0.05mol O2����C��ȷ��
D���ơ������ơ��������ƺ�ˮ��Ӧ�ķ���ʽ�ֱ����£�
Na+H2O=NaOH+
�����Ѷȣ�һ��
2��ѡ���� ��0.5 mol����0.5 molþ�ֱ����2 mol��L��1��400 mL�������У�������Һ��������
A����������Һ��������
B��ͬ����
C������þ��Һ��������
D����ȷ��
�ο��𰸣�B��?
����������ɷ�Ӧ����ʽ֪�����߾������������
2Na��2H��===2Na����H2��������m
2 mol? 44 g
0.5 mol? 11 g
Mg��2H��===Mg2����H2��������m
1 mol? 22 g
0.5 mol? 11 g
��Һ����������ȡ������������������(��m)���йؽ������ᷴӦ������Һ�����������⡣
�����Ѷȣ�һ��
3��ʵ���� Ϊ��̽���Ҵ��ͽ����Ʒ�Ӧ��ԭ�������������ĸ�ʵ�飬�ش��������⣺
ʵ��һ����С�ձ��м�����ˮ�Ҵ����ٷ���һС������ƣ��۲������ռ����������� ��
��
ʵ������跨����ʵ��һ�ռ��������塣
ʵ���������Թ��м���3 mLˮ��������һС������ƣ��۲�����
ʵ���ģ����Թ��м���3 mL���ѣ�������һС������ƣ��۲�����
��1������ʵ����м��������ʵ�鷽���������жϵ����� ????????????
????????????
��2���ӽṹ�Ϸ�������ʵ��ѡȡˮ���������������ԭ����??????????
��3��ʵ������Ŀ������֤��???��ʵ���ĵ�Ŀ������֤��??????������ʵ������ʵ���ĵĽ��������֤���Ҵ��ͽ����Ʒ�Ӧ�Ļ�ѧ����ʽӦΪ???????????
�ο��𰸣���1�����ռ��������ȼ������ȼ�ջ��ܸ���������֤������������
�����������
�����Ѷȣ�һ��
4��ʵ���� ��13�֣�����֬�ް�סԼ0.2g�������Ʒ�ĩ������ʯ�����ϣ�����֬���ϵ�ˮ���۲쵽��֬����ȼ��������
��1��������ʵ���������õ����йع������Ƹ�ˮ��Ӧ�Ľ����ǣ���һ�����������ɣ��ڶ���??????????��Na2O2��ˮ��Ӧ�Ļ�ѧ����ʽ��???????????????��
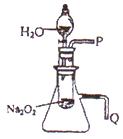
��2��ij�о���ѧϰС��������ͼ��ʾװ�ã����������ã�����ʵ�飬��֤���������ۡ�������֤��һ�����۵�ʵ������������ǣ�???????????��������֤�ڶ������۵�ʵ������������ǣ�??????????????????????��
��3�����Թ��м�ˮ��������ȫ�ܽ��Ҳ������������ɺ�ȡ���Թܣ����Թ��е����̪��Һ��������Һ�ȱ�����ɫ��Ϊ̽����ԭ��С��ͬѧ�Ӳ����й������е�֪��Na2O2��ˮ��Ӧ������H2O2��H2O2����Ư���ԡ�
�����һ����ʵ�飬��֤Na2O2������ˮ��ַ�Ӧ�����Һ����H2O2���ڡ���ֻҪ��д��ʵ�����õ��Լ����۲쵽������
�Լ���??????????????????????��
����??????????????????????��
��4����С��ͬѧ����ö����ķ���̽��Na2O2��ˮ��Ӧ�����Һ���Ƿ���H2O2����ʵ�鷽��Ϊ����ȡ2.6g Na2O2���壬ʹ֮��������ˮ��Ӧ����������O2�������������ֵ�Ƚϣ����ɵó����ۣ�

�ٲ����������ʱ��������Թܺ���Ͳ�ڵ����嶼��ȴ������ʱ���У�Ӧѡ����ͼװ���еģ����Ե�������Ͳ����ռ�������???????����A��B����������??????????��
�����ڱ�״���²�������������Ӧѡ�õ���Ͳ�Ĵ�С���Ϊ??????��ѡ�100mL������200mL������500mL����1000mL����
�ο��𰸣�
 �����������
�����������
�����Ѷȣ�һ��
5��ʵ���� ��ʵ����ģ�ҵ����̼���ƣ�һ���¶��£���һ��������NaCl��Һ��ͨ�백���ﵽ���ͺ��ٲ���ͨ��CO2��һ��ʱ����ֳ��������˵õ�NaHCO3���塣
��1���ù��̵Ļ�ѧ����ʽ��????????????????????????????????????????????????��
��2������NaHCO3�õ�������Ʒ��ʵ���ҿɽ��д˲�����װ����???????????��
 ?
?
A????????????????? B???????????????? C???????????????????? D
��3���õ��Ĵ�����Ʒ��������NaHCO3��NaCl�����ʵ����֤��Ʒ�и�����֡��Լ���������ѡ�ã��Թܡ���ͷ�ιܡ�����װ�á�Ba(NO3)2��Һ��NaOH��Һ��AgNO3��Һ������ʯ��ˮ��ϡ���ᡢϡ���ᡢϡ���ᡣ
����һ��ȡ������Ʒ���Թ��У�����������ˮ�����ܽ⡣���Թ��м���????????????
???????????????????????????���۲�?????????????????
| ������Һ�в���������ɫ������
���ۣ�????????????????????????????��
|
�������������һ����Һ���ˣ�ȡ��Һ���Թ���B�У�����???????????????????????��
���۲�
| ?
����???????????????????????????��
���ۣ���Ʒ�к���NaHCO3��
|
�������������������Һ���ˣ�ȡ��Һ���Թ�C�У�?????????????????????????????
??????????????????????????���۲�
| ?
����???????????????????????????��
���ۣ�????????????????????????????��
?
��4���õ�������������ˮ�в�����Cl2��Ũ�ȣ�
�� �ڴ���ƿ�з��ù�����KI����һ�����ı����ᣬȷȡˮ��200mL����ƿ�У�Ѹ������ƿ��ҡ����ˮ���ʵ���ɫ��������Ӧ��Cl2+2I��=2Cl��+ I2��
�ڼ�����������Һ����cmol/L Na2S2O3��Һ�ζ���������Ӧ��I2+2S2O32��=2I��+S4O62������????????????????????????????????????????????????????????????���ﵽ�ζ��յ㡣
���ظ�����3�Σ�ƽ������ΪV mL�������Ʒ�в���Cl2��Ũ�ȣ�?????????mg/L��Cl�����ԭ��������35.5��
�ο��𰸣���16�֣�
��1�� NaCl + NH3 + CO2
���������
�����������1�����������ڱ���ʳ��ˮ����NH3+H2O=NH3?H2O���õ��Ȼ��ơ���ˮ��Һ��һˮ�ϰ������������̼���������������ͨ�������̼����ʱ��NH3?H2O+CO2=NH4HCO3������̼�����Ƶ��ܽ�ȱ��Ȼ��ơ�̼����臨�С��̼���������ȴﵽ���ͣ���̼��������Ȼ�������Ӧ������̼�����ƾ�����Ȼ����Һ����NH4HCO3+NaCl=NaHCO3��+NH4Cl������������Ӧ�������ɵã�NaCl + NH3 + CO2 + H2O = NaHCO3 ��+ NH4Cl����2��̼�������ǹ���
�����Ѷȣ�����
|