微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 关于图-1中各装置的叙述不正确的是(???)
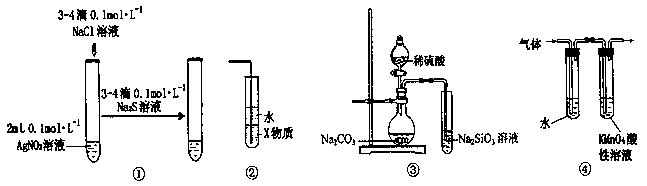
A.装置①能验证AgCl沉淀可转化为溶解度更小的Ag2S沉淀
B.装置②中X若为四氯化碳,可用于吸收氨气,并防止倒吸
C.装置③的实验可推断硫、碳、硅三种元素的非金属性强弱
D.装置④可检验溴乙烷发生消去反应得到的气体中含有乙烯
参考答案:A
本题解析:A项中所给AgNO3的量明显过量,银离子可直接与硫离子生成硫化银沉淀,并不能证明溶解平衡的转化,不正确
B:氨气并不与水直接接触,可防止倒吸,正确
C:烧瓶中生成CO2,试管中有硅酸沉淀生成,由强酸制弱酸可以证明酸性硫酸>碳酸>硅酸,进而可证明非金属性:硫>碳>硅,正确
D:溴乙烷发生消去反应可得到乙烯与溴化氢,溴化氢由水吸收后,乙烯可使KMnO4溶液褪色,正确
答案为A
本题难度:一般
2、选择题 下列实验中说法正确的是
A.蒸发操作中,应使混合物中的水未完全蒸干时,就停止加热
B.将饱和FeCl3溶液滴入煮沸的NaOH溶液中,从而制得Fe(OH)3胶体
C.过滤操作不能用来分离胶体和溶液
D.开始蒸馏时,应该先加热蒸馏烧瓶,再开冷凝水;蒸馏完毕,应该先关冷凝水再撤酒精灯
参考答案:AC
本题解析:略
本题难度:简单
3、选择题 下列各组物质,不用任何试剂即可鉴别开来的是( )
A.NaCl、NaBr、KI三种无色溶液
B.HCl、NaCl、NaNO3、Na2CO3四种溶液
C.NaBr、HCl、KCl三种溶液
D.淀粉、淀粉碘化钾、碘化钾、溴水四种溶液
参考答案:A.三种无色溶液相互滴加都不反应,没有明显的现象,不能鉴别,
本题解析:
本题难度:一般
4、选择题 某同学想用实验证明FeCl3溶液显黄色不是氯离子造成的,下列实验无意义的是
A.观察KCl溶液没有颜色
B.向FeCl3溶液中滴加适量NaOH溶液,振荡静置,过滤后所得滤液黄色消失
C.向FeCl3溶液中滴加适量AgNO3溶液,振荡静置,过滤后所得滤液黄色未消失
D.加水稀释后FeCl3溶液黄色变浅
参考答案:D
本题解析:
试题分析:氯化钾溶液中存在的离子有:钾离子、氯离子、水分子,可以与氯化铁溶液中的离子分析比较,得出显色的是铁离子,故A正确,氯化铁与氢氧化钠反应生成了氢氧化铁沉淀和氯化钠,将铁离子转化成了沉淀,只有氯离子和水分子留下来了,得出显色的是铁离子,故B正确,加入硝酸银后将氯离子转化为沉淀,但溶液的黄色未消失,可以得出显色的不是氯离子而是铁离子,故C正确,加水后改变了氯化铁溶液的浓度,而对离子不会造成消除,故D错误。所以选D。
本题难度:一般
5、实验题 (10分)研究碳及其化合物的利用对促进低碳社会的构建具有重要的意义。某学习小组查阅资料并进行相关探究,请帮忙完成以下探究。
(1)pC类似于pH,是指极稀溶液中的溶质浓度的常用对数的负值。如某溶液中某溶质的浓度为1×10-3 mol/L,则该溶液中该溶质的pC=-lg(1×10-3)=3。如图为25℃时H2CO3溶液的pC-pH图。请回答下列问题:(若离子浓度小于10-5mol/L,可认为该离子不存在)
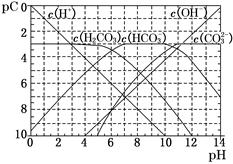
①在同一溶液中,H2CO3、HCO3-、CO32-________(填“能”或“不能”)大量共存。
②H2CO3一级电离平衡常数的数值Ka1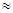 ????????。
????????。
③人体血液里主要通过碳酸氢盐缓冲体系(H2CO3/HCO3-)可以抵消少量酸或碱,维持pH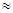 7.4。当过量的酸进入血液中时,血液缓冲体系中的c(H+)/c(H2CO3)最终将????????。
7.4。当过量的酸进入血液中时,血液缓冲体系中的c(H+)/c(H2CO3)最终将????????。
A.变大
B.变小
C.基本不变
D.无法判断
(2)高温时,用CO还原MgSO4可制备高纯MgO。由MgO可制成“镁―次氯酸盐”燃料电池,其装置示意图如图,
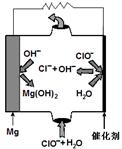
该电池反应的离子方程式为????????????????????????????????。
(3)二氧化碳合成甲醇是碳减排的新方向,将CO2转化为甲醇的热化学方程式为: CO2(g) +3H2(g)  ?CH3OH(g) +H2O(g)? △H ;
?CH3OH(g) +H2O(g)? △H ;
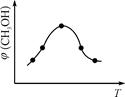
①取五份等体积CO2和H2的混合气体(物质的量之比均为1∶3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH)与反应温度T的关系曲线如图
所示,则上述CO2转化为甲醇反应热ΔH????????0(填“>” “<”或“=”)。
②一定温度下,在容积相同且固定的两个密闭容器中,按如下方式投入反应物,一段时间后达到平衡。
容?器
| 甲
| 乙
|
反应物
投入量
| 1molCO2
3molH2
| a molCO2、b molH2、
c molCH3OH(g)、c molH2O(g)
若甲中平衡后气体的压强为开始时的0.8倍,要使平衡后乙与甲中各物质浓度相同,且起始时维持反应逆向进行,则c的取值范围为???????????????。
参考答案:(共10分)
(1)①不能 ?(1分) ②10-6
本题解析:
试题分析:(1)①:H2CO3会发生电离出H+, HCO3-会发生电离出H+和发生水解结合H+, CO32-会发生水解与H+结合,故H2CO3、HCO3-、CO32-不能大量共存。②分析图中可以看到当PH=6时H2CO3发生一极电离,因此Ka1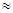 10-6。③过量的酸含有大量的H+,因此c(H+)/c(H2CO3)最终将变大。 10-6。③过量的酸含有大量的H+,因此c(H+)/c(H2CO3)最终将变大。
(2)由图中分析得出,Mg是负极,失去电子,生成Mg(OH)2,ClO-会得到电子生成Cl-,因此电池反应的离子方程式为:Mg + ClO- + H2O = Cl- + Mg(OH)2。
(3)①由图可知最高点反应到达平衡,达平衡后,温度越高,φ(CH3OH)越小,平衡向逆反应进行,升高温度平衡吸热方向进行,逆反应为吸热反应,则正反应为放热反应,即△H3<0。
故答案为:<。
②根据分析化学方程式,反应前后的化学总物质的量之比是2:1,又因为甲中平衡后气体的压强为开始时的0.8倍,因此c的最小量为0.8/[(1mol+3mol)/2]=0.4mol,最大值为1mol,故c的取值范围为:0.4<c≤1。
点评:(1)本题考查弱电解质在水溶液中的电离及图象,学生能正确了利用图象来分析是解答本题的关键,并注意利用习题中的信息来解答,难度不大.(2)本题从多个角度对化石燃料进行了全面的考查,难度中等,培养了学生分析问题解决问题的能力.
本题难度:一般
|