微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 室温时,下列各组离子在指定溶液中可以大量共存的是
A.由水电离出的c(H+)=10-12mol/L的溶液中:Na+、Ba2+、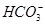 、Cl-
、Cl-
B.无色透明溶液中:K+、Cu2+、SO42-、Na+
C.含有大量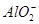 的溶液中:Na+、OH-、Cl-、
的溶液中:Na+、OH-、Cl-、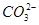
D.能使pH试纸显红色的溶液中:Na+、ClO-、Fe2+、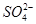
参考答案:C
本题解析:A项,该溶液呈酸性或碱性,无论该溶液呈酸性还是呈碱性,碳酸氢根离子都不能大量共存。B项,铜离子呈蓝色。D项,使pH试纸显红色的溶液显酸性,酸性条件下,次氯酸根离子有强氧化性,能氧化二价铁离子,所以不能共存。
本题难度:一般
2、选择题 在强酸性溶液中能大量共存的无色透明离子组是( )
A.K+??Na+???NO3-??CO32-
B.Mg2+??Na+???Cl-??SO42-
C.K+??Na+?? Cl-?? Cu2+
D.Na+Ba2+OH-??SO42-
参考答案:A.因H+、CO32-结合生成水和气体,则不能共存,故A错误
本题解析:
本题难度:一般
3、选择题 在水溶液中能大量共存的一组离子是( )
A.Al3+、Na+、HCO3-、SO42-
B.H+、Fe2+、ClO-、Cl-
C.Mg2+、K+、SO42?、NO3-
D.NH4+??Ag+、OH-、Br-
参考答案:A.Al3+与HCO3-发生互促水解反应而不能大量共存,故A
本题解析:
本题难度:一般
4、填空题 (12分)某强酸性溶液X中仅含有Ba2+、Al3+、NH4+、Fe2+、Fe3+、CO32-、SO32-、SO42-、Cl-、NO3-中的一种或几种,取该溶液进行连续实验,实验过程如下:

根据以上信息,回答下列问题:
(1)仅根据上述连续实验不能确定溶液X中是否含有的阳、阴离子分别是_____________。
(2)用离子方程表达下列反应:
①中生成气体A:___________ __。
②中生成溶液H:____________ _。
(3)若②中所用氢氧化钠浓度为2mol/L,当加入l0 ml时开始产生沉淀,55 ml时沉淀的量达到最大值0.03 mol,继续滴加沉淀的量保持不变,随后再滴加沉淀部分溶解,到60ml时沉淀的量降为0.025 mol且保持不变,则原溶液中c(Fe2+)为___________mol/L、c(Fe3+)为___________mol/L、c(Cl-)为___________mol/L。(若有些离子不存在,请填0 mol/L)
参考答案:(每空2分共14分)(1) Fe3+、Cl-
本题解析:
试题分析:强酸性溶液中一定不存在CO32-、SO32-,则与过量的硝酸钡溶液反应,生成9.32g沉淀,则该沉淀是硫酸钡沉淀,物质的量是9.32g/233g/mol=0.04mol,说明溶液中存在0.04mol SO42-,则一定不存在Ba2+;与过量硝酸钡反应生成的气体A可连续被氧化,说明A是NO,D是二氧化氮,则溶液中存在与硝酸发生氧化还原反应的离子,为Fe2+,所以溶液中一定不存在NO3-;溶液B中含有铁离子和过量的硝酸钡,加入氢氧化钠溶液仍产生气体,说明原溶液中存在NH4+,氨气的物质的量也是铵根离子的物质的量是0.112L/22.4L/mol=0.005mol;则沉淀G中一定含有氢氧化铁;通入过量的二氧化碳,仍能产生沉淀,因为铁离子上步中被完全沉淀,所以此时产生的沉淀只能是氢氧化铝,说明溶液中存在铝离子;而Fe3+、Cl-不能确定。
(1)根据以上分析,不能确定溶液X中是否含有的阳、阴离子分别是Fe3+、Cl-;
(2)①硝酸与亚铁离子发生氧化还原反应生成铁离子、NO和水,离子方程式是3Fe2++4H++NO3-=3Fe3++NO↑+2H2O;
②中生成溶液H,即为铝离子和过量的氢氧化钠反应生成偏铝酸钠和水,离子方程式是Al3+ +4OH-=AlO2-+2H2O;
(3)根据生成NO的体积可计算亚铁离子的浓度,NO的物质的量是0.112L/22.4L/mol=0.005mol,则亚铁离子的物质的量是0.005mol×3=0.015mol,c(Fe2+)=0.015mol/0.1L=0.15mol/L;加入氢氧化钠溶液60mL时沉淀量降到0.025mol,说明此时为氢氧化铁沉淀,亚铁离子的物质的量是0.015mol,所以说明原溶液中存在铁离子,其物质的量是0.025mol-0.015mol=0.01mol,则c(Fe3+)=0.01mol/0.1L=0.1mol/L;加入55mL氢氧化钠溶液时沉淀达到最大值0.03mol,加入60mL氢氧化钠溶液时,沉淀降为0.025mol,说明氢氧化铝的物质的量是0.03mol-0.025mol=0.005mol,则溶液中SO42-:0.04mol,NH4+:0.005mol,Fe2+:0.015mol,Fe3+:0.01mol,Al3+:0.005mol,此时2n(SO42-)=n(NH4+)+2n(Fe2+)+3n(Fe3+)+3n(Al3+),所以c(Cl-)=0mol/L。
考点:考查离子的检验与计算
本题难度:困难
5、选择题 下列各组离子在指定溶液中能大量共存的是
A.常温下,呈碱性的溶液:K+、AlO2-、CO32-、Na+
B.含Fe3+的溶液中:K+、NH4+、Cl-、I-
C.中性溶液:Fe3+、Al3+、NO3-、SO42-(已知:Fe3+沉淀的pH的范围在2.7~3.7)
D.无色溶液中:K+、AlO2-、NO3-、HCO3-
参考答案:A
本题解析:
试题分析:离子间如果发生化学反应,则不能大量共存,反之是可以的。A、溶液显碱性,则K+、AlO2-、CO32-、Na+可以大量共存,A正确;B、Fe3+和I-发生氧化还原反应2Fe3++2I-=I2+2Fe2+,二者不能大量共存,B不正确;C、根据Fe3+沉淀的pH的范围在2.7~3.7可知,在中性溶液中Fe3+不能大量共存,C不正确;D、在溶液中AlO2-与HCO3-不能大量共存,二者发生反应AlO2-+HCO3-+H2O=Al(OH)3↓+CO32-,D不正确,答案选A。
本题难度:一般