微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 不能用金属跟氯气直接反应制得的氯化物的是?
A.NaCl
B.MgCl2
C.CuCl2
D.FeCl2
参考答案:D
本题解析:
试题分析:氯气具有强氧化性,和铁反应生成的是氯化铁,答案选D。
点评:本题是基础性试题的考查,知识点属于记忆性的,关键是学生要熟练记住常见元素及其化合物的有关转化。
本题难度:简单
2、实验题 已知Cl2和碱溶液在不同条件下,得到的产物不同。某兴趣小组用下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。(3Cl2+6KOH KClO3+5KCl+3H2O )
KClO3+5KCl+3H2O )
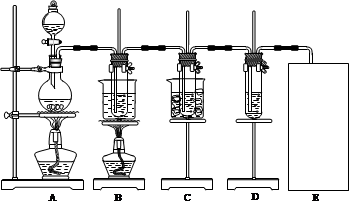
图中:A为氯气发生装置;B的试管里盛有15 mL 30% KOH溶液,并置于水浴中;C的试管里盛有15 mL 8% NaOH溶液,并置于冰水浴中;D的试管里加有紫色石蕊试液。请填写下列空白:
(1)制取氯气时,在圆底烧瓶里加入一定质量的二氧化锰,通过?????????????(填仪器名称)向圆底烧瓶中加入适量的浓盐酸。装置A中反应的离子方程式为???????????????????。需要向烧瓶中加碎瓷片吗????????????(选填:“需要”、“不需要”)。
(2)反应结束后,烧瓶里的溶液??????????。
A一定显酸性;B可能显酸性,也可能为中性;C只有氧化性;D只有还原性;E既有氧化性又有还原性
(3)反应完毕,B试管中有少量晶体析出,经冷却后,有大量晶体析出。图中符合该晶体溶解度曲线的是??????(填编号字母);从B的试管中分离出该晶体必须用到的玻璃仪器有??????????????????????????????。
来源:91考试网 91EXAm.org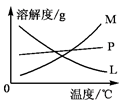
(4)该小组同学发现制得的氯酸钾产量偏低,可能的一种原因是Cl2中含有HCl气体。对此问题可以通过改进实验装置的方法进行避免。方法是???????????????????????????。
(5)实验中可观察到D的试管里溶液的颜色由紫色先变为_________色,最终变为________色。
(6)C装置中反应完毕的现象是______________________________________________。
(7)请在装置图方框中画出缺少的实验装置,并注明试剂。
参考答案:分液漏斗(1分);MnO2+4H++2Cl-![]()
本题解析:
试题分析:(1)向烧瓶中加热浓盐酸,需要借助于分液漏斗。在加热的条件下二氧化锰氧化浓盐酸生成氯气,反应的离子方程式为MnO2+4H++2Cl- Mn2++Cl2↑+2H2O;由于在反应中二氧化锰不溶于水,以固体的形式存在,因此反应中不需要再加热碎瓷片。
Mn2++Cl2↑+2H2O;由于在反应中二氧化锰不溶于水,以固体的形式存在,因此反应中不需要再加热碎瓷片。
(2)由于在反应过程中浓盐酸的浓度逐渐降低,而
本题难度:一般
3、选择题 将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO3-两种离子的物质的量(n)与反应时间(t)的变化示意图如右图所示。下列说法正确的是
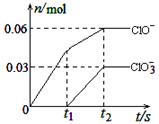
A.苛性钾溶液中KOH的物质的量是0.09mol
B.ClO3-的生成是由于氯气的量的多少引起的
C.在酸性条件下ClO-和ClO3-可生成Cl2
D.反应中转移电子的物质的量是0.21mol
参考答案:D
本题解析:根据图像可知反应后,生成KClO和KClO3分别是0.06mol和0.03mol,则根据电子的都是守恒可知,生成氯化钾是0.06mol×1+0.03mol×5=0.21mol。所以D正确,A不正确,应该是0.3mol。B不正确,应该和温度有关系;C不正确,两种离子不可能都得到电子,答案选D。
本题难度:一般
4、选择题 用漂白粉溶液浸泡过的有色布条,如果晾置在空气中,过了一段时间,其漂白效果会更好的原因可能是
A.漂白粉被氧化了
B.漂白粉跟空气中的 CO2反应充分,生成了较多量的 HClO
C.有色布条被空气中的氧气氧化了
D.漂白粉溶液蒸发掉部分水,其浓度增大
参考答案:B
本题解析:
试题分析:漂白粉有效成分是Ca(ClO)2,在空气中发生反应Ca(ClO)2+CO2+H2O=CaCO3↓+ 2HClO,次氯酸起到漂白作用。
本题难度:一般
5、实验题 (8分)欲用密度为1.18g/cm3(质量分数36.5%)的浓盐酸配制250mL1mol/L盐酸,回答下列各问:
(1)所需浓盐酸体积约为_______mL(填整数)。
(2)所需仪器为量筒、烧杯、滴管及_____、_______。
(3)若定容时俯视,所配溶液的物质的量浓度比要求的值________(填“偏高”或“偏低”)。
(4)若定容后再摇匀静置,发现凹液面低于刻度线。此时应该(填标号)_____。
A. 直接转移到试剂瓶中? B. 加水重新定容后贮存于容量瓶中
C. 重新定容后再转移到试剂瓶中
参考答案:(1)21
(2)玻璃棒、250mL容量瓶
(3
本题解析:略
本题难度:简单