微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列装置或操作不能达到的实验目的是[???? ]
A.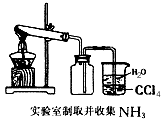
B.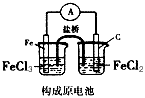
C.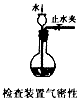
D.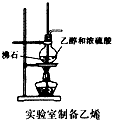
参考答案:B
本题解析:
本题难度:一般
2、实验题 一般情况下,当人体一次性摄取300mg~500mg亚硝酸钠时,就会引起中毒。某研究小组用碘量法测定泡菜中亚硝酸盐的含量。有关反应如下:
2NaNO2+2H2SO4 +2KI==K2SO4 +I2+2H2O+Na2SO4 +2NO
I2 +2Na2S2O3==2NaI+Na2S4O6
取1kg泡菜,榨汁,将榨出的液体收集后,加入提取剂和氢氧化钠,使得到的泡菜汁中的亚硝酸盐都成为亚硝酸钠。在过滤后的滤液中加入氢氧化铝乳液,以除去色素。再次过滤后得到滤液,将该滤液稀释至
1L,取 25. 00mL稀释后的滤液与过量的稀硫酸和碘化钾溶液反应,再选用合适的指示剂,用0.05000
mol・L-1的 Na2S2O3标准溶液进行滴定。数据记录如下;
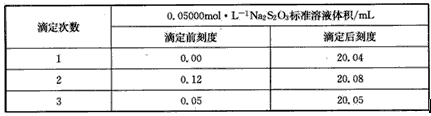
请回答下列问题:
(1)该实验中可选用的指示剂是___,滴定终点的现象是____。
(2)有经验的厨师在做泡菜时往往加入适量的橙汁,以减轻亚硝酸盐的危害。这主要是因为橙汁中含有丰富 的维生素C,维生素C具有___性(填“氧化性”或“还原性”)。
(3)通过计算判断若某人一次食入0.125kg这种泡菜,是否会引起中毒__________。
参考答案:(1)淀粉;蓝色刚好褪去,且30s不恢复
(2)还原性
本题解析:
本题难度:一般
3、实验题
|
为除去粗盐中的Ca2+、Mg2+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量)

(1)判断BaCl2已过量的方法是_____________________。
(2)第④步中,写出相应的化学方程式(设粗盐溶液中Ca2+的主要存在形式为CaCl2) ;
___________________________________.
(3)在 中填写所使用除杂试剂的化学式__________,在( )中的操作名称是_______。
中填写所使用除杂试剂的化学式__________,在( )中的操作名称是_______。
(4)从实验设计方案优化的角度分析步骤②和④可否颠倒____________(填“是”或“否”,如果“否”,请说明理由。)原因是:_____________________;步骤③和④可否颠倒____________。
(5)若先用盐酸再进行操作⑤,将对实验结果产生影响,其原因是:____________________________
参考答案:(1)取第②步后的上层清液1~2滴于点滴板上(或取少量上层清
本题解析:
本题难度:一般
4、实验题 黄铜矿是工业炼铜的主要原料,主要成分为CuFeS2,含少量脉石。为测定该黄铜矿的纯度,某同学设计了如下实验:

现用电子天平称取研细的黄铜矿样品1.150g,在空气存在下进行煅烧,生成Cu、Fe3O4和
SO2气体,实验后取d中溶液的1/10置于锥形瓶中,用0.05mol/L标准碘溶液进行滴定,消耗标准碘溶液20.00mL。请回答下列问题:
(1)将样品研细后再进行反应,其目的是____________;标准碘溶液应盛放在_______(填“碱式”或“酸式”)?滴定管中。
(2)装置a的作用是_____________。
A.除去空气中的二氧化碳???????B.除去空气中的水蒸气 ?
C.有利于气体混合?????????????D.有利于观察、控制空气流速
(3)若去掉c装置,会使测定结果________(填“偏低”、“偏高”或“无影响”),写出影响测定结果的化学方程式?____________________。
(4)上述反应结束后,仍需通一段时间的空气,其目的是___________________。
(5)通过计算可知,该黄铜矿的纯度为_____________。
(6)假设实验操作均正确,测得的黄铜矿纯度仍然偏低,可能的原因主要有___________。
参考答案:(1)使原料充分反应、加快反应速率;酸式
(2)BD<
本题解析:
本题难度:一般
5、实验题 过氧化氢是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用作消毒、杀菌、漂白等。某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量,并探究了过氧化氢的性质。
Ⅰ.测定过氧化氢的含量请填写下列空白:
(1)移取10.00 m密度为ρ g/mL的过氧化氢溶液至250mL_______(填仪器名称)中,加水衡释至刻度,摇匀。移取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样。
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请将相关物质的化学计量数及化学式填写在横线上。
____MnO4-+____H2O2+____H+=____Mn2++____H2O+________
(3)滴定时,将高锰酸钾标准溶液注入______(填“酸式”或“碱式”)滴定管中。滴定到达终点的现象是________________。
(4)反复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数
为____________。
(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果________(填“偏高”或“偏低”或“不变”)。
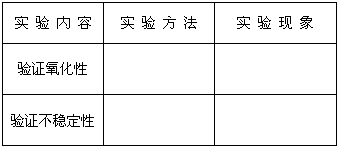
Ⅱ.探究过氧化氢的性质该化学举小组根据所提供的实验条件设计了两个实验,分别证明了过氧化氢的氧化性和不稳定性。(实验条件:试剂只有过氧化氢溶液、氯水、碘化钾演粉溶液、饱和硫化氢溶液,实验仪器及用品可自选。)请将他们的实验方法和实验现象填入下表
(6)
参考答案:(1)容量瓶
(2)2、5、6、2、8、5O2
本题解析:
本题难度:一般