��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���Ե�ؾ��������ŵ��������ص㣬����õ��㷺Ӧ�ã�п-�̸ɵ����KOH��ҺΪ���Һ������ܷ�ӦʽΪ��Zn��s��+2MnO2��s��+H2O��l��=Zn��OH��2��s��+Mn2O3��s������˵��������ǣ�������
A����ع���ʱ��пʧȥ����
B�����·��ÿͨ��0.2mol���ӣ�п�����������ϼ���6.5g
C����������ĵ缫��ӦʽΪ��2MnO2��s��+H2O��l��+2e-=Mn2O3��s��+2OH-
D����ع���ʱ������������ͨ����������
�ο��𰸣�D
���������
�����Ѷȣ�һ��
2��ѡ���� ���й�����ͼ��ʾ��ԭ��ص��й�˵���У���ȷ���ǣ�������
A��Zn�Ǹ�����������ԭ��Ӧ
B��Cu�Ǹ���������������Ӧ
C��пƬ���������ݳ�
D��������пƬͨ����������ͭƬ
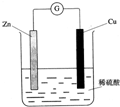
�ο��𰸣�A��Zn�Ǹ���������������Ӧ����A����
B��Cu����
���������
�����Ѷȣ���
3��ѡ���� X��Y��Z��M�������ֽ���Ԫ�ء�����X��Z�õ������ӷ���ϡ������ʱ��Z������H2�ų��������Y2+��Z2+�������Һʱ��Y����������֪M2+��������ǿ��Y2+���������ֽ����Ļ����ǿ������˳��Ϊ��������
A��X>Z>Y>M
B��X>Y>Z>M
C��M>Z>X>Y
D��X>Z>M>Y
�ο��𰸣�D
���������
�����������������֪������X��Z�õ������ӷ���ϡ������ʱ��Z�����������ų�����X�Ǹ�����Z�������������Ļ��X��Z�������Y2+��Z2+���ӹ������Һʱ��Y��������˵��Y2+������ǿ��Z2+�������Ļ��Z��Y��M2+���ӵ�������ǿ��Y2+���ӣ������Ļ��Y��M���������������ֽ����Ļ����ǿ������˳��ΪX��Z��Y��M��ѡD��
���㣺���������ԱȽϡ�ԭ���ԭ���͵��ԭ����Ӧ�á�
�����Ѷȣ�һ��
4��ѡ���� ��26�֣�����ͼװ�ý���ʵ�飬���ش��������⣺
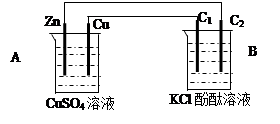
��1���ж�װ�õ����ƣ�A��Ϊ___________ ��B��Ϊ______________��
��2��п��Ϊ________�����缫��ӦʽΪ???????????????????????????????????��
ͭ��Ϊ________�����缫��ӦʽΪ???????????????????????????????????��
ʯī��C1Ϊ______�����缫��ӦʽΪ??????????????????????????????????��
ʯī��C2����������ʵ������Ϊ??????????????????????????????????????��
��3����C2������224mL���壨��״̬��ʱ��п�������仯_________���������С����________g��CuSO4��Һ������_________�����ӡ��������٣�_________g��
�ο��𰸣���1��ԭ��أ�����
��2������? Zn��2e-=Z
���������
�����������1���������װ��֪��AΪԭ��أ�BΪ���أ���2��AΪԭ��أ����������Խ�ǿ��пΪ�������缫��ӦʽΪZn-2e-=Zn2+�����������Խ�����ͭΪ�������缫��ӦΪ��Cu2++2e-=Cu��ʯī��C1��ԭ��ص���������Ϊ���ص�������������������ʧ���������������缫��ӦʽΪ��2Cl--2e-=Cl2����ʯī��C2��ԭ��صĸ�������Ϊ���ص��������缫��ӦʽΪ2H��+2e-=H2�������������������������������ӣ���Һ�ʱ�죻��3��ʯī��C2��ԭ��صĸ�������Ϊ���ص��������缫��ӦʽΪ2H��
�����Ѷȣ�һ��
5���ж��� ��10�֣��������վñ������ɫ�����������������������������ԭ���ԭ�����С���?�⡱ ��?�䴦������Ϊ����һ��Ũ�ȵ�ʳ����Һ����һ���������У��ٽ���ڵ�����������Һ�У�����һ��ʱ���ɫ����ȥ�����ָ������Ҳ�����ʧ���Իش�
��1��ʳ�ε�������??????????????????????��
��2���ڴ�ԭ��ط�Ӧ�У����������ĵ缫��ӦΪ?????????�����������ĵ缫��ӦΪ?????????��
��3����Ӧ�����в�����������ζ�����壬��Һ�з����ķ�ӦΪ?????????��ԭ����ܷ�Ӧ����ʽΪ??????????????��
��4��ʵ�ʲ����У�����ʳ��ˮʱ��ͨ��������һ������С�մ�����Ҫ������??????????????����һ��Ӧ�Ļ�ѧ����ʽ��???????????????????????��
�ο��𰸣���1���������������
��2��2Al-6e-�T�T2A
�����������1���γ�ԭ�����Ҫ����ʵ��磬���NaCl��������������á�
��2�����������Ϣ����ɫ��ȥ����������ʧ�������뷢��Ag2S Ag�仯��
Ag�仯��
���������ã�Ϊ������ʧ���ӱ��Al3+,��ӦΪ��Al-3e-�T�TAl3+��Ag2S��ΪAg��S2-���õ��ӣ���ԭ��ص���������ӦΪ��Ag2S+2e-�T�T2Ag+
�����Ѷȣ���