微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 关于下列图示的说法中正确的是(???)
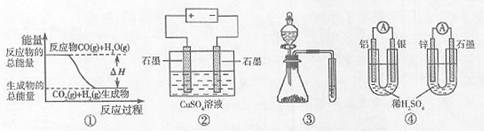
A.图①表示可逆反应:“CO(g)+H2O(g)  CO2(g)+H2(g)”中的△H大于0
CO2(g)+H2(g)”中的△H大于0
B.图②为电解硫酸铜溶液的装置,一定时间内,两电极产生单质的物质的量之比一定为1:1
C.图③实验装置可完成比较乙酸、碳酸、苯酚酸性强弱的实验
D.图④两个装置中通过导线的电子数相同时,消耗负极材料的物质的最也相同
参考答案:C
本题解析:略
本题难度:简单
2、选择题 铅蓄电池是最常见的二次电池,下列有关该电池的说法错误的是( )
A.该电池的正极板上覆盖有PbO2,负极板上覆盖有Pb
B.该电池放电时的正极反应为PbO2(s)+4H+(aq)+SO42-(aq)+ 2e-=PbSO4(s)+2H2O(l)
C.该电池充电时,两个电极上都有PbSO4生成
D.用该电池电解饱和食盐水制氯气,若制得0.050molCl2,这时电池内消耗H2SO40.10mol
参考答案:解;A、铅蓄电池负极材料为Pb,发生氧化反应,正极材料为Pb
本题解析:
本题难度:简单
3、选择题 为增强铝的耐腐蚀性,现以铅蓄电池为外电源,以Al作阳极、Pb作阴极,电解稀硫酸,使铝表面的氧化膜增厚。其反应原理如下:
电池: Pb(s) + PbO2(s) + 2H2SO4(aq) =2PbSO4(s) + 2H2O(l);
电解池:2Al+3H2OAl2O3+3H2↑电解过程中,以下判断正确的是:
?
| ??????????电池
| ?????????????电解池
|
A
| H+移向Pb电极
| H+移向Pb电极
|
B
| 每消耗3molPb
| 生成2molAl2O3
|
C
| 正极:PbO2+4H++2e―=Pb2++2H2O
| 阳极:2Al+3H2O-6e―=Al2O3+6H+
|
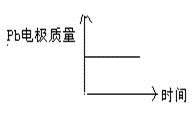
D
| 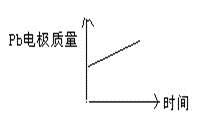
| 
?
参考答案:D
本题解析:铅蓄电池负极为Pb,Pb-2e-+SO42-=PbSO4;
正极是PbO2,PbO2+2e-+SO42-+4H+=PbSO4+2H2O。
阴离子向负极移动,阳离子向正极移动;两极质量均增加。
电解池中,阳极Al,2Al+3H2O-6e-=Al2O3+6H+;
阴极Pb,6H++6e-=3H2;
每消耗3Pb,生成1mol Al2O3。答案选D。
本题难度:一般
4、填空题 (12分)(1).下列有关电化学的图示中,完全正确的是?????????????
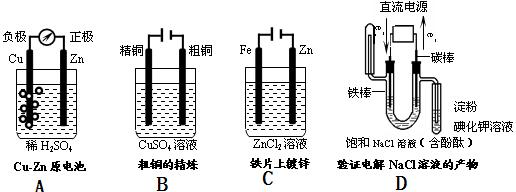
(2).碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病。碘酸钾(KIO3)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水。碘酸钾在酸性介质中可与碘化物作用生成单质碘。以碘为原料,通过电解制备碘酸钾的实验装置如图所示。
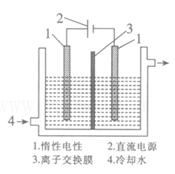
请回答下列问题:
a、碘是?????????(填颜色)固体物质,实验室常用???????方法来分离提纯含有少量泥沙杂质的固体碘。
b、电解前,先将一定量的精制碘溶于过量氢氧化钾溶
液,溶解时发生反应:3I2+6KOH==5KI+KIO3+3H2O,
将该溶液加入阳极区。另将氢氧化钾溶液加入阴极区,电解槽用水冷却。
电解时,阳极上发生反应的电极反应式为????????,每生成1mol KIO3,电路中通过的电子的物质的量为___________________。
c、电解过程中,为确定电解是否完成,需检验电解液中是否有I-。请设计一个检验
电解液中是否有I-的简单实验方案,并按要求填写下表。
可供选择的试剂有淀粉溶液,稀硫酸,氯化钠溶液,酒精等。(用其中的一种或多种均可。)
实验方法
| 实验现象及结论
| ?
| ?
d、电解完毕,从电解液中得到碘酸钾晶体的实验过程如下:
阳极电解液→①蒸发浓缩→②→③过滤→④洗涤→⑤→碘酸钾晶体
步骤②的操作名称是??????????????,步骤⑤的操作名称是????????。步骤④洗涤
晶体的目的是?????????????????。
参考答案:(12分)
a、紫黑色(1分)升华(或加热)(1分)b
本题解析:略
本题难度:一般
5、选择题 关于下列四个图像的说法中正确的是
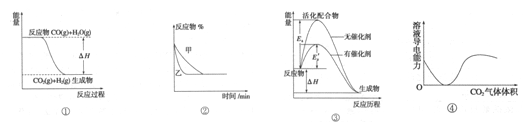
A.图①表示可逆反应CO(g)+H20(g)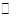 5C02 (g)+H2 (g)△H>0 5C02 (g)+H2 (g)△H>0
B.图②表示压强对可逆反应2A(g)+2B(g) 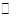 3C(g)+D(s)影响,乙的压强大 3C(g)+D(s)影响,乙的压强大
C.图③表示有无催化剂化学反应中能量变化
D.图④表示C02通人饱和碳酸钠溶液中,溶液导电性变化
参考答案:C
本题解析:A 错误表示的反应是放热反应,△H<0
B 错误2A(g)+2B(g)  ?3C(g)+D(s)改变压强,平衡会移动,图像中甲、乙平衡之后的反应物的百分含量不会相等。 ?3C(g)+D(s)改变压强,平衡会移动,图像中甲、乙平衡之后的反应物的百分含量不会相等。
C 正确使用催化剂,会降低反应的活化能
D 错误溶液中始终都存在钠离子,导电能力不可能为零。
本题难度:简单
|
|