��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��ͼ��ʾ�ļס��ҡ������־���
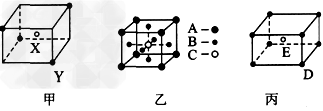
?���ƶϼ��廯ѧʽ��XΪ�����ӣ�Ϊ____���Ҿ�����A��B��C�������ĸ�������
____����������ÿ��D����Χ���E���ĸ�����________����
�ο��𰸣�X2Y��1:3:1��8
���������
�����Ѷȣ�һ��
2������� ��15�֣�Ѫ�����к���C��O��N��Fe����Ԫ�ء��ش��������⣺
��C��N��O��H����Ԫ���е縺����С����?????????????����Ԫ�ط��ϣ���д����̬Feԭ�ӵĺ�������Ų�ʽ??????????��
����ͼ��ʾΪѪ�쵰�ͼ��쵰�Ļ��Բ��֨D�DѪ���صĽṹʽ��Ѫ������Nԭ�ӵ��ӻ���ʽ��????????????������ͼ�ķ������á��������Fe2������λ����
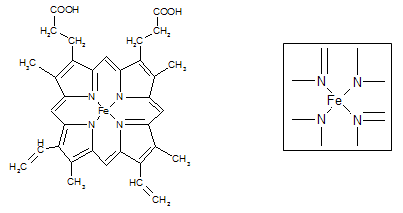
��NiO��FeO�ľ���ṹ���;����Ȼ��Ƶ���ͬ��Ni2+��Fe2+�����Ӱ뾶�ֱ�Ϊ69 pm��78 pm�����۵�NiO ________ FeO(�<����>��)��
��N��H�γɵĻ�������(N2H4)���������ȼ�ϣ�ȼ��ʱ�����ķ�Ӧ�ǣ�
 ???
???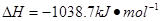
���÷�Ӧ����4mol N��H�����ѣ����γɵ� ����___________mol��
����___________mol��
�ɸ��ݵȵ���ԭ����д��CN���ĵ���ʽ???????�� 1 mol O22+�к��еĦм���ĿΪ?????��
�����Цġ��á�������ͬ�������壬�þ��徧���������е���ԭ����Ϊ???���ġ������־�������ԭ�ӵ���λ��֮��Ϊ???��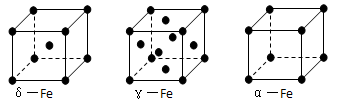
�ο��𰸣���H ��1�֣�?? [Ar]3d64S2��2�֣�
��s
�����������1���ǽ�����Խǿ���縺��Խ����H�����ݹ���ԭ����д����̬Feԭ�ӵĺ�������Ų�ʽ��
��2�����ݽṹͼ�ɿ���Nԭ�Ӽ��е�������˫�������Լ���sp2�ӻ�������sp3�ӻ���Nԭ��������й¶Ե��ӣ����������������ɵ��ӵĿչ�������Կ��γ���λ����
��3�����Ӿ��������Ӽ�Խǿ���۷е�Խ�ߣ��γ����Ӽ������뾶ԽС�����������Խ�࣬���Ӽ�Խǿ������NiO�� FeO�ġ�
��4����Ӧ����4mol N��H�����ѣ�������1.5mol����������������2�� �����Ѷȣ���
�����Ѷȣ���
3��ѡ���� ����˵������ȷ���ǣ�??��
A��ˮ����ȴ��00C����ʱ��ɱ�������Ϊˮ���Ӵ�Һ�����˹���
B�������������¶ȱ仯ʱ���ܱ��ֳ���̬�仯
C���������¶ȣ�ֻ����ѹǿ��Ҳ����ʹ���ʴ�������Һ��
D�������ܹ�������������Ϊ������������ܹ���������
�ο��𰸣�C
���������ˮ�����Dz���仯�ģ�ѡ��A����ȷ�������ʱ��������������ѡ��B����ȷ��ѡ��D����ȷ��Ӧ������֮��ľ��뷢���˱仯�����Դ�ѡC��
�����Ѷȣ���
4������� ��8�֣�����ѧ??�����ʽṹ�����ʡ�
�����й�֪ʶ�ش��������⣺
��1��B��F��Ԫ���γɵĻ�����Ŀռ乹��Ϊ??????��������ԭ�ӵ��ӻ�����Ϊ????????��
��2��CH4��??????��д�����ţ���Ϊ�ȵ����塣
��3��д��Ԫ��Cu��̬ԭ�ӵĵ����Ų�ʽ???????????????????????��
��4��Fe��CO���γɵ�Fe��CO��5�ͻ�����û����ﳣ���³�Һ̬���۵�Ϊ��20.5�棬�е�Ϊ103�棬�����ڷǼ����ܼ����ݴ˿��жϸû����ᄃ������??????���壨������ͣ���
��5��Zn�����ӵ��������ﲻ����ˮ���������ڰ�ˮ�У���������NH3���ϵ�������Ϊ???????????��
��6������Fe�ľ����ڲ�ͬ�¶��������ֶѻ���ʽ�������ֱ�����ͼ��ʾ��������������������������������ʵ�ʺ��е�ԭ�Ӹ���֮��Ϊ?????��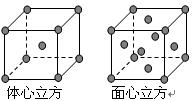
�ο��𰸣�
(���һ��2�֣�����ÿ��1��)
��1��ƽ������
�����������
�����Ѷȣ�һ��
5��ѡ���� ԭ�Ӽ��Թ��۵��������ķǽ��������У�һ��ԭ��������ԭ�ӵijɼ���Ϊ8-N��NΪ�÷ǽ���Ԫ�ص�����������ѧ�Ұ���һ�����Ϊ8-N����ij�ǽ������ʵĽṹ��ͼ��ʾ���ɸõ��ʵ�Ԫ��λ�ڣ�������
A����A
B����A
C����A
D����A
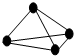
�ο��𰸣�C
���������
�����Ѷȣ�һ��