��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ����������SnSO4�������ڶ�����ҵ��ijС�����SnSO4�Ʊ�·��Ϊ��
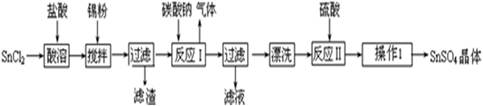
�������ϣ�
�����������£�����ˮ��Һ����Sn2+��Sn4+������Ҫ������ʽ��Sn2+�ױ�������
��SnCl2��ˮ�����ɼ�ʽ�Ȼ�����
��1����ԭ�ӵĺ˵����Ϊ50����̼Ԫ��ͬ����A�壬��λ�����ڱ��ĵ�?????���ڣ�1�֣�
��2���������� ???????????????���ˡ�ϴ�ӵȣ�2�֣�
��3���ܽ�SnCl2��ĩ���Ũ���ᣬԭ����??????????????????????????????????????????????????
��4������Sn�۵��������������ٵ�����ҺpH?��???????????????????????????????????
��5����Ӧ��õ�������SnO���õ��ó��������ӷ�Ӧ����ʽ��??????????????????????????????????????
��6�����������£�SnSO4��˫��ˮȥ��Ӧ�����ӷ���ʽ��??????????????????????????????????????????
��7����С��ͨ�����з����ⶨ�������۵Ĵ��ȣ����ʲ����뷴Ӧ����
�ٽ��������������У������ķ�ӦΪ��Sn+2HCl�TSnCl2+H2����
�ڼ��������FeCl3��
������֪Ũ�ȵ�K2Cr2O7�ζ������ɵ�Fe2+���ټ������۵Ĵ��ȣ�����ƽ����ʽ��
FeCl2 +???K2Cr2O7 +???HCl = ?????FeCl3 + ?????KCl + ????CrCl2+????
�ο��𰸣�32.��16�֣���1���������ڣ�1�֣���??��2������Ũ����
���������
�������: �⣺��1����Ԫ����̼Ԫ������ͬһ���壬���ڢ�A�壬ԭ�Ӻ˵����Ϊ50����50-2-8-8-18=14����Sn���ڵ������ڡ�
��2��������ͼ��֪���������Ǵ���Һ�еõ����ᾧˮ�ľ��壬ֻ�ܲ�ȡ����Ũ������ȴ�ᾧ�����ˡ�ϴ�ӵõ���
��3������Ϣ��֪��SnCl2��ˮ�����ɼ�ʽ�Ȼ�����������ˮ��ƽ��SnCl2+H2O �����Ѷȣ�����
�����Ѷȣ�����
2��ѡ���� ���ϲ��ϵ�ʹ��ʹ������������˺ܴ����ߣ�����Ҫԭ������
[???? ]
A�����ϲ��ϵ�ʹ�ÿ���ʹ�����ܾ��ܳ����µı仯
B�����ϲ��ϵ�ʹ�ÿ���ʹ��������������
C�����ϲ��ϵ�ʹ�ÿ���ʹ�������ܳ���ǿ�ȵĸı�
D�����ϲ��ϵ�ʹ�ÿ���ʹ���������¶ȵľ��ұ仯
�ο��𰸣�B
���������
�����Ѷȣ���
3������� ��ʯΪ�����Σ���ѧʽ��Ca2Mg5Si8O22��OH��2����д����������ʽΪ______��
�ο��𰸣������θ�д����������ʽʱ�����õĽ���������д��ǰ�棬��дSi
���������
�����Ѷȣ���
4��ѡ���� �����йغ�ˮ�ۺ����õ�˵������ȷ��
A��������������ӽ����ȷ���������ˮ
B����ˮ����ֻ�漰�����仯
C�����ú�ˮ������ȡ����Mg
D������������Դ��������������Ϊ����
�ο��𰸣�B
���������
�����������ˮ���εķе�ߣ�ˮ�ķе�ϵͣ���˿���������ˮ�ķ�����ȡ����ˮ��Ҳ���������ӽ����ķ�����ȥ��ˮ�е��������ӣ���ȡ��ˮ��A����ȷ����ˮ����Ԫ���ԣ�1����ʽ���ڣ�Br2����Ԫ����0����ʽ���ڣ���ˮ����һ�������������ɣ�һ���漰��ѧ�仯��������ԭ��Ӧ��B���ȷ����ˮ�к���+2�۵�þԪ�أ�ͨ�������ᴿ�����Ʊ���ˮMgCl2���壬����þ�ǻ��ý����������õ������MgCl2�ķ�����ȡ����þ��������C����ȷ������������ԴʱҪ���������������ƻ�������D����ȷ��
�����Ѷȣ���
5������� ��ҵ���Ի�����Ϊԭ������������Ҫ��Ϊ�����ν��У������ա������������ա���ش��������⣺
(1)���ջ������γɵ�¯�����뾭������ϴ�ӡ���������???????????(���豸����)������ҪĿ����????????????????��
(2)��������ʹ�õĴ�������ý(V2O5)�ܼӿ���������������ʣ��˹����в�����һ�������м���(��ͼ1)

����a��c������Ӧ�Ļ�ѧ����ʽ�ɱ�ʾΪ��???????????��?????????��
(3)550��ʱ��SO2ת��ΪSO3��ƽ��ת����(��)����ϵ��ѹǿ(P)�Ĺ�ϵ��ͼ2��ʾ��
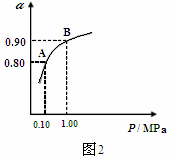
��2.0mol SO2��1.0mol O2����5L�ܱ������У���Ӧ��ƽ�����ϵ��ѹǿΪ0.10M Pa��A��B��ʾ��ͬѹǿ�µ�SO2ת���ʣ�ͨ������¹�ҵ�����в��ó�ѹ��ԭ���ǣ�?��Դ:91���� ��??????��
(4)Ϊѭ�����ô�����������Ա����������һ�����ӽ��������շ����¹��գ������ʴ�91.7%���ϡ���֪�Ϸ������к���V2O5��VOSO4�������Բ�������������֪��VOSO4������ˮ��V2O5������ˮ��NH4VO3������ˮ���ù��յ�������ͼ���£�
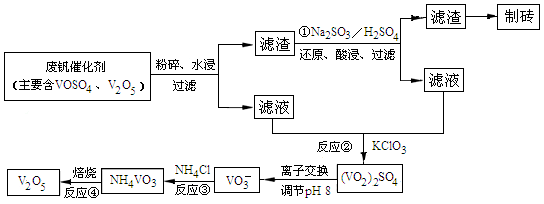
��Ӧ�٢ڢۢ�������������ԭ��Ӧ����???????????(���������)����Ӧ�ٵ����ӷ���ʽΪ???????????????????????????????????????���ù����з�Ӧ�۵ij�����(�ֳƳ�����)�ǻ��շ��Ĺؼ�֮һ�������ʵĸߵͳ�����ҺpHӰ���⣬����Ҫ�����Ȼ��ϵ��(NH4Cl������������Һ��V2O5��������)���¶ȡ�������ͼ�Խ�������Ȼ��ϵ�����¶ȣ�???????????��???????????��
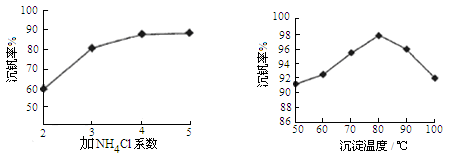
�ο��𰸣�(1)�Ӵ���???��ֹ�����ж�
(2)SO2+V2O
���������(1)������ȼ�����ɵĶ�����������Ϊ��ֹ�����ж�������������ϴ�ӡ���������Ӵ��Ҵ�����Ϊ��������
(2)����֪��Ϣ֪��V2O5������ã�a��V2O5�����V2O4��˵��V���ϼ۽��ͣ�����SԪ�صĻ��ϼ����ߣ������ķ�Ӧ��SO2+V2O5 SO3+V2O4��ͬ����c�У�V�Ļ��ϼ����ߣ���OԪ�صĻ���
SO3+V2O4��ͬ����c�У�V�Ļ��ϼ����ߣ���OԪ�صĻ���
�����Ѷȣ�����