微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 实验室用Al2(SO4)3制取Al(OH)3,最合适的试剂是??????? (??? )
A.NaOH
B.H2SO4
C.NH3?H2O
D.KOH
参考答案:C
本题解析:由于氢氧化铝可溶于强碱,故用铝盐制取Al(OH)3时,一般选用弱碱,例如氨水
本题难度:简单
2、选择题 把镁粉中混有少量的铝粉除去,应选用的试剂是
A.稀盐酸
B.烧碱溶液
C.硫酸铝溶液
D.氨水
参考答案:B
本题解析:
试题分析:A、镁和铝都是活泼的金属,都能和酸反应,A不正确;B、铝能溶解在强碱氢氧化钠溶液中,镁与氢氧化钠溶液不反应,因此把镁粉中混有少量的铝粉除去,应选用的试剂是氢氧化钠溶液,即烧碱溶液,B正确;C、镁能和硫酸铝发生置换反应生成硫酸镁和铝,因此C不正确;D、氨水是弱碱,与铝不反应,D不正确,答案选B。
本题难度:简单
3、选择题 H2SO4、Al2(SO4)3和MgSO4的混合溶液中,加入NaOH溶液时,其沉淀的质量W和加入的NaOH体积V之间的关系如图所示,则原混合溶液中Al3+、Mg2来源:91exam .org+和SO42―的物质的量之比为(?)
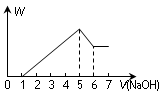
A.1∶1∶1
B.5∶3∶2
C.2∶1∶5
D.3∶2∶2
参考答案:C
本题解析:
试题分析:H2SO4、Al2(SO4)3和MgSO4的混合溶液中,加入NaOH溶液时,先发生的是酸碱中和,然后产生了氢氧化铝和氢氧化镁沉淀,最后氢氧化铝溶解,其离子方程式分别为
H++OH-=H2O、Al3++4OH-=AlO2-+2H2O、Mg2++2OH-=Mg(OH)2↓,由图可以知道,设1V积极的氢氧化钠的含量为amol,刚开始为酸碱的中和,所以酸的物质的量为0.5amol,因为Al(OH)3+OH-=AlO2-,有图可以知道铝的物质的量为amol,所以消耗镁的氢氧化钠为6amol-
本题难度:一般
4、简答题 将0.1mol镁、铝合金溶于100mL2mol/L的H2SO4溶液中,然后滴加1mol/L的NaOH溶液,生成沉淀与所加NaOH溶液体积的关系如图所示.试回答下列问题:
(1)当溶液中Mg2+、Al3+恰好沉淀完全时,V(NaOH)=______mL;
(2)当V1=160mL时,金属粉末中镁的物质的量为多少?此时V2的值又是多少?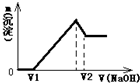
参考答案:将镁、铝合金溶于H2SO4溶液中,发生反应:Mg+H2SO4
本题解析:
本题难度:一般
5、选择题 铝制器皿能够盛放的物质是 [???? ]
A.KOH溶液????
B.浓硫酸????
C.NaOH溶液????
D.稀硫酸
参考答案:B
本题解析:
本题难度:简单