微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列各组离子在无色透明的酸性溶液中能大量共存的是
A.Mg2+、Al3+、SO42-、Cl-
B.Na+、Ca2+、NO3-、CO32-
C.Na+、Cl-、K+、Cu2+
D.Na+、HCO3-、CO32-、K+
参考答案:A
本题解析:
试题分析:A、这些无色离子在酸性条件下可以共存,正确;B、CO32-、H+不能大量共存,错误;C、Cu2+有颜色,错误;D、HCO3-、CO32-、H+不能共存,错误。
考点:考查离子共存问题。
本题难度:一般
2、计算题 Ⅰ.某溶液中仅含下表离子中的5种离子(不考虑水的电离及离子的水解),且离子的物质的量均为1mol。
阴离子
| SO42-、NO3-、Cl-
|
阳离子
| Fe3+、Fe2+、NH4+、Cu2+、Al3+
①若向原溶液中加入KSCN溶液,无明显变化。②若向原溶液中加入过量的盐酸,有气体生成,溶液中阴离子种类不变。③若向原溶液中加入BaCl2溶液,有白色沉淀生成。试回答下列问题
(1)若先向原溶液中加入过量的盐酸,再加入KSCN溶液,现象是 。
(2)原溶液中含有的阳离子是 。
(3)向原溶液中加入足量的盐酸,发生反应的离子方程式为 。
(4)向原溶液中加入足量的NaOH溶液,充分反应后,过滤、洗涤、灼烧,最终所得固体用托盘天平称量质量为 。
Ⅱ. 草酸亚铁晶体(FeC2O4・2H2O)、碳酸锂和二氧化硅在氩气中高温反应可制备锂电池的正极材料硅酸亚铁锂(Li2FeSiO4)。草酸亚铁晶体在氩气气氛中进行热重分析,结果如右图所示(TG%表示残留固体质量占原样品总质量的百分数),请回答下列问题:

(5)草酸亚铁晶体中碳元素的化合价为:
(6)A→B发生反应的化学方程式为 。
(7)精确研究表明,B→C实际是分两步进行的,每一步只释放一种气体,第二步释放的气体的相对分子质量较第一步的大,则第一步释放的气体化学式为: ;释放第二种气体时,反应的化学方程式为 。
参考答案:(16分,每空2分)(1)溶液呈红色(2分) &#
本题解析:
试题分析:Ⅰ.若向溶液中加入KSCN溶液,无明显变化,说明原溶液中不含Fe3+;若向溶液中加入过量的盐酸,有气体生成,溶液中阴离子种类不变,说明原溶液中含有Cl-,该气体只能是NO,说明含有具有氧化性的NO3-和具有还原性的Fe2+。若向溶液中加入BaCl2溶液,有白色沉淀生成,说明原溶液中含有SO42-。各离子的物质的量均为1mol,因此根据电荷守恒可知还应含有Cu2+,所以原溶液中所含阳离子是Fe2+、Cu2+,阴离子是NO3-、Cl-、SO42-。
(1)如果先加入盐酸,在酸性条件下NO3-具有氧化性,能和具有还原性的Fe2+发生氧化还原反应,反应的离子方程式为3Fe2++4H++NO3-=3Fe3++NO↑+2H2O。所以再滴入KSCN溶液,溶液呈红色。
(2)原溶液中含有的阳离子是Fe2+和Cu2+。
(3)根据以上分析可知,向原溶液中加入足量的盐酸,发生反应的离子方程式为3Fe2++4H++NO3-=3Fe3++NO↑+2H2O。
(4)原溶液中所含阳离子是Fe2+、Cu2+,若向原溶液中加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧至恒重,最终得到的固体应该是是CuO、Fe2O3。根据题意各离子的物质的量均为1mol可知,m(CuO)=1.0mol×80g/mol=80.0g,m(Fe2O3)=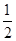 ×1.0mol×160g/mol=80.0g,所得固体的质量为80.0g+80.0g=160.0g。 ×1.0mol×160g/mol=80.0g,所得固体的质量为80.0g+80.0g=160.0g。
Ⅱ.(5)草酸亚铁晶体(FeC2O4・2H2O)中铁元素的化合价是+2价,氧元素是-2价,所以碳元素的化合价是(2×4-2)÷2=+3价。
(6)根据草酸亚铁晶体的化学式FeC2O4・2H2O可知,晶体中结晶水的含量是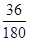 ×100%=20%,所以A→B发生反应恰好是失去结晶水,因此反应的化学方程式为FeC2O4・2H2O ×100%=20%,所以A→B发生反应恰好是失去结晶水,因此反应的化学方程式为FeC2O4・2H2O FeC2O4 +2H2O。 FeC2O4 +2H2O。
(7)草酸亚铁晶体中FeO的含量是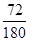 ×100%=40%,所以C点生成的固体是氧化亚铁。由于第二步释放的气体的相对分子质量较第一步的大,所以第一步释放的是CO,第二步释放的是CO2,反应的化学方程式分别是FeC2O4 ×100%=40%,所以C点生成的固体是氧化亚铁。由于第二步释放的气体的相对分子质量较第一步的大,所以第一步释放的是CO,第二步释放的是CO2,反应的化学方程式分别是FeC2O4 FeCO3+CO、FeCO3 FeCO3+CO、FeCO3 FeO + CO2↑。 FeO + CO2↑。
考点:考查离子共存和检验;方程式的书写;化学计算;化合价的判断以及物质含量的有关计算和判断
本题难度:困难
3、选择题 下列各组离子在指定条件下,一定能大量共存的是(????)
①能使红色石蕊试纸变蓝的溶液中:K+、Na+、CO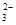 、NO3-、AlO2- 、NO3-、AlO2-
②c(H+)=10-1mol・L-1的溶液中:Cu2+、Al3+、SO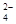
③能使碘化钾淀粉试纸变蓝的溶液中:Na+、NH、S2-、Br-
④水电离出的c(H)=10-13mol・L-1的溶液中:Na+、Mg2+、Cl-、SO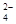
⑤在加入铝粉能产生H2的溶液中: NH4+、Fe2+、SO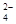 、NO3― 、NO3―
⑥在含大量Fe3+的溶液中:NH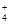 、Na+、Cl-、SCN- 、Na+、Cl-、SCN-
A.①②
B.①③
C.②④
D.①②⑤⑥
参考答案:A
本题解析:①说明是碱性溶液;②表明为酸性溶液;③说明溶液具有强氧化性,故还原性较强的S2-、Br-不可能存在;④水的电离受抑制,故溶液可能是强酸性,也可能为强碱性,而Mg2+在碱性环境中不可能大量存在;⑤加入铝粉能产生H2的溶液同样说明溶液即可为强酸性,也可为强碱性,很明显不合题意;⑥Fe3+与SCN-可形成络合物
本题难度:一般
4、选择题 在下列给定的溶液中,一定能大量共存的离子组是(???)
A.过量Al与NaOH溶液反应所得溶液中:K+、Cl-、Al3+、SO42-
B.常温下,OH-的浓度为10-11mol/L的溶液中:Na+、I-、NH4+、NO3-
C.常温下,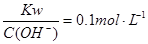 的溶液中:K+、NH4+、Cl-、SO42- 的溶液中:K+、NH4+、Cl-、SO42-
D.与Al反应产生H2的溶液中:K+、Na+、I-、NO3-
参考答案:C
本题解析:
试题分析:A项:Al与NaOH溶液反应生成的AlO2-离子会和Al3+发生双水解,故不能共存;B项:OH-的浓度为10-11mol/L的溶液呈酸性,在酸性条件下,NO3-有很强的氧化性,能氧化I-,故不能共存;D项:与Al反应产生H2的溶液既可以呈酸性又可以呈碱性,在酸性条件下,NO3-有很强的氧化性,能氧化I-,故不能共存。故选C。
点评:本题考查离子的共存问题,熟悉离子的性质及发生的反应是解答本题的关键,难度不大。(1)离子间相互结合形成沉淀、气体、弱电解质、络离子时不能大量共存;离子间
本题难度:一般
5、选择题 在由水电离产生的C(H+)=1×10-14mol・L-1的某无色溶液中一定能大量共存的是
A.Fe2+、K+、SO42-、NO3-
B.Mg2+、NH4+、SO42-、Cl-
C.Na+、K+、SO42-、NO3-
D.Ba2+、Na+、SO42-、MnO4-
参考答案:C
本题解析:水电离产生的C(H+)=1×10-14mol・L-1则该溶液可能为强酸性溶液或强碱性溶液,A中Fe2+与强碱溶液生成氢氧化亚铁沉淀, Fe2+在强酸性溶液中与NO3-发生氧化还原反应,(B)中NH4+与强碱溶液中生成氨气不能共存。(D)中MnO4-为紫红色
本题难度:一般
|