��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ʵ���� ��ʯ����Ҫ�ɷ�ΪCaC2������ΪCaO��CaS���ǹ�ҵ����Ȳ�ij���ԭ�ϣ�ij�о���ѧϰС�������������ַ����ⶨCaC2��������������������и��⡣
����һ����ȡ1.40 g��Ʒ��Բ����ƿ�У��÷�Һ©������������ˮ��ʹ��Ʒ��Ӧ��ȫ������������ɫ
���徭Bϴ����ͨ������װ�ò����Ȳ�������Ϊ��״����448 mL����������Ȳ��ˮ�е��ܽ⣬
��ͬ����
��1����ʯˮ��������Ȳ����Ļ�ѧ����ʽΪ��???????????????????????????????
��2��������װ���ʵ��Լ��Ĺ��ƿ������˫���������������ɣ��������ʵ���װ�ã�����ͼ�н��䲹����������ע�����ƿ��װ���Լ������ơ�

��3���Ի��ȷ�������������IJ�����????????????????������ţ�
�ټ��װ�õ������ԣ�
�ڻָ������º������µ�����Ͳλ�ã�ʹC��D��Һ����ƽ��
����Aװ�ý�����������һ�����ܣ�ͨ��N2��A��C2H2ȫ�����뵽B��C�У�
�ܶ���ʱ��������Ͳ�ڰ�Һ����͵���ƽ
��4�����������ݿɼ������Ʒ��CaC2����������Ϊ____?????��
����������ȡl.40g��Ʒ����ͼ��ʾʯӢ���У��гּ�����װ��ʡ�ԣ�����a�����ϻ���ͨ���������
������ʯӢ���е���Ʒ����Ӧ��ȫ����ñ���Һ�������ȷ�Ӧǰ������1.80g����Ӧ����ʽΪ��2CaC2+
5O2��2CaO+ 4CO2��

��5����Ӧ��ɺ�ʯӢ������Ʒ����ܱڲ�����ʴ�����û�ѧ����ʽ������ԭ��????????????
��6������ƿ�����Ը��������Һ������Ϊ???????????????????????????????????????????
��7���ɴ˷�����õ���Ʒ��CaC2�����������ȷ���һ�е�____??????????�������С������
�ȡ�������ʵ��װ�õĽǶȿ���ԭ��Ϊ??????????????????????????????????????????????��
�ο��𰸣���1��CaC2+2H2O��Ca(OH)2+C2H2����2�֣�
���������
�����������1����ʯ��ˮ��Ӧ����̼���ƺ���Ȳ����˵�ʯˮ��������Ȳ����Ļ�ѧ����ʽΪCaC2��2H2O��Ca(OH)2��C2H2����
��2���������ɵ���Ȳ�����к������ʣ������Ҫ��������ͭ��Һ������������Һ��ȥ����Ȳ���ܶȺͿ����ܽӽ���һ������ˮ���ռ���������ȷ��������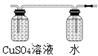 ��
��
��3���ټ��װ�õ������ԣ����Է�ֹ���ɵ���Ȳ��ʧ����˶Ի��ȷ������������棻�ڻָ������º������µ�����Ͳλ�ã�ʹC��D��Һ����ƽ����ʹ����ѹǿ��ȣ��Ի��ȷ������������棻�����ڷ�Ӧǰװ���оʹ��ڿ�����������Aװ�ý�����������һ�����ܣ�ͨ��N2��A��C2H2ȫ�����뵽B��C�жԻ��ȷ������������棻�ܶ���ʱ��������Ͳ�ڰ�Һ����͵���ƽ�Ի��ȷ������������棬��˴�ѡ�ۡ�
��4����Ȳ�����ʵ�����0.448L��22.4L/mol��0.02mol������ݷ���ʽ��֪̼���Ƶ����ʵ���Ҳ��0.02mol����������0.02mol��64g/mol��1.28g������̼���Ƶ�����������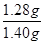 ��100%��91.43%��
��100%��91.43%��
��5������̼�������ɵ��������Ǽ���������ܺͲ����еĶ������跴Ӧ���ɹ���ƣ��Ӷ���ʴ�ܱڣ���Ӧ�Ļ�ѧ����ʽ��CaO + SiO2 CaSiO3��
CaSiO3��
��6�����ڵ�ʯ�к�������Ԫ��S�ȣ��ڷ�Ӧ������SO2��Ҳ�ܱ�����������Һ���ո���CO2�IJ�����������Ҫ���Ը��������Һ��ȥCO2�л��е�SO2���������塣
��7�����ڿ�����Ҳ����CO2�����a��ͨ�����ʱ��ȱһ��ϴ��װ�ã����¿����е�CO2Ҳ�������գ�ʹ�������ƫ��
�����Ѷȣ�һ��
2��ѡ���� ����������һ��2008-2009ѧ���һѧ�ڸ����ڶ��ο��ԣ���ѧ��3�����л�ѧʵ����������У���ȷ����
A��������Һʱ������Ͳ��Һ�嵹���ձ���Ӧ����Ͳϴ�ӣ���ϴ��ҺҲ�����ձ�
B��ϡ��Ũ����ʱ����Ũ������������ʢ��ˮ���ձ��в����Ͻ���
C���ø����pH��ֽ�ֱ��1 mol��L��1��NaOH��Һ��1 mol��L��1��H2SO4��pHֵ
D����ƾ��ƼӾƾ�ʱ��Ӧ���Լ�ƿ�еľƾ�ֱ�ӵ���ƾ�����
�ο��𰸣�B
�����������Ͳֻ�Ǵ�����ȡҺ�����������������ϴ�ӣ�pH��ֽ��õ�ֵ��Χ��1��14����������ͨ������1 mol��L��1��H2SO4��pHֵӦС��0����ƾ��ƼӾƾ�ʱ��Ӧ����ͨ©����ƾ����мӾƾ���
�����Ѷȣ�һ��
3��ѡ���� ����ͼ��ʾװ�ý�������ʵ�飬�ܴﵽʵ��Ŀ�ĵ���?? (����)��
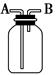
A��ƿ��ʢ������ŨH2SO4����A�ڽ���������NH3
B����B�ڽ��������ſ������ռ�CO2
C��ƿ��ʢ��ˮ����B�ڽ���������ˮ���ռ�NO2
D��ƿ��װ��ˮ��A�����ӵ��ܲ�������Ͳ�У���B�ڽ���������ˮ����������H2�����
�ο��𰸣�D
���������A�������ŨH2SO4����NH3��B��������ſ������ռ�CO2ʱ��Ӧ��A�ڽ�����C�NO2��H2O��Ӧ����������ˮ���ռ���D�H2������ˮ����B�ڵ���H2���ܽ�ƿ��ˮѹ����Ͳ�У��Ӷ�����H2�������
�����Ѷȣ�һ��
4��ѡ���� ��һ֧50mL��ʽ�ζ�����ʢ���ᣬҺ��ǡ����a mL�̶ȴ����ѹ���Һ��ȫ���ų���ʢ����Ͳ�ڣ�����Һ�����һ����
A��a mL
B��(50�Da)mL
C������(50�Da)mL
D������a mL
�ο��𰸣�C
���������
����������ζ��ܵġ�0���̶����϶ˣ����̶����¶ˣ��ζ��̶ܿ�ֵ���ϵ��¿̶������ζ������̶����»���һ�οռ�û�п̶ȣ�50mL�ζ�����ʵ��ʢ��Һ����������50mL����ˣ�һ֧50mL��ʽ�ζ�����ʢ���ᣬҺ��ǡ����a mL�̶ȴ����ѹ���Һ��ȫ���ų����������̶����µ���Һһ���ų�����������(50�Ca)mL��ʢ����Ͳ�ڣ�����Һ�����һ���Ǵ���(50�Ca)mL����ѡC��
�����Ѷȣ���
5��ѡ���� ����ʵ���Ӧ�Ľ�����ȷ����
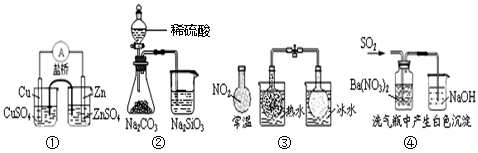
A���������Zn��Cuԭ���
B������֤���ǽ����ԣ�S��C��Si
C����˵����Ӧ2NO2 N2O4��H��0
N2O4��H��0
D���� ��ɫ����ΪBaSO3
�ο��𰸣�AB
���������
���������ͭ��ͭ����Һ��п��п����Һ�����š��������пͭԭ��أ���A����ȷ���μ�ϡ���ᣬ�ų����壬�ձ������ɰ�ɫ������˵�����ԣ�H2SO4>H2CO3>H2SiO3����ǽ����ԣ�S>C>Si����B����ȷ����ͼ��֪������ƽ��������NO2�ķ����ƶ�������ƽ��������N2O4�ķ����ƶ���������Ӧ�Ƿ��ȷ�Ӧ�����H<0����C�����SO2�����ᱵ��Һ����ΪSO42����SO42����Ba2+���ΪBaSO4����D�����
�����Ѷȣ�һ��