��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� �ྦྷ��(�赥�ʵ�һ��)����Ϊ�����Ӵ��õĻ�ʯ�����Ʊ��и�������SiCl4Ϊ�������Ի�����Ⱦ�ܴ�����ˮǿ��ˮ�⣬�ų��������ȡ��о���Ա����SiCl4ˮ�����ɵ�����ͱ����(��Ҫ�ɷ�ΪBaCO3���Һ��иơ�����þ������)�Ʊ�BaCl2��2H2O������������ͼ��ʾ����֪������Fe3����Mg2����ȫ������pH�ֱ���3.4��12.4��
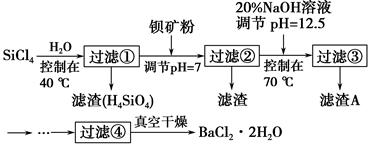
(1)SiCl4ˮ�������40 ���ԭ����___________________________________��
��֪��SiCl4(s)��H2(g)=SiHCl3(s)��HCl(g)?��H1����47 kJ��mol��1
Si(s)��3HCl(g)=SiHCl3(s)��H2(g)?��H2����189 kJ��mol��1
����SiCl4�Ʊ�����Ȼ�ѧ����ʽΪ__________________________________��
(2)�ӱ����ʱ����BaCl2�����ӷ�Ӧ����ʽ��_________________________��
(3)��20% NaOH��Һ����pH��12.5���õ�����A����Ҫ�ɷ���________�������¶�70 ���Ŀ����____________________________________________��
(4)BaCl2��Һ������Ũ�������½ᾧ�����ˣ��پ���ո����õ�BaCl2��2H2O��ʵ����������Ũ�����õ��ĺ������ε�������__________�֡�
(5)Ϊ���ָù��յ���ɫ��ѧ˼�룬�ù�������ѭ�����õ�������____________��
�ο��𰸣�(1)��ֹHCl�ӷ���Ⱦ���������SiCl4��ˮ�����ʣ���ֹ
�������������������ϢSiCl4��ˮ��Ӧʱ��ǿ��ˮ�Ⲣ�ų��������ȣ������¶Ƚϵͣ����Խ��ͷ�Ӧ���ʣ�����HCl�Ļӷ���������������Ȼ�ѧ����ʽ�������õ��ƹ���Ȼ�ѧ����ʽ��(2)���˺���ҺΪ���ᣬ��̼�ᱵ������Ӧ��̼�ᱵ���ܣ�д���ӷ���ʽʱ��Ӧ������ѧʽ��(3)�������е���Ϣ��������Fe3����Mg2����ȫ������pH�ֱ���3.4��12.4����˵���pH��7ʱ��������Ҫ�ɷ���Fe(OH)3��pH��12.5ʱ��������Ҫ�ɷ���Mg(OH)2��ͬʱ�����¶Ƚϸ�ʱ��Ca(OH)2�ܽ�ȼ�С����Ca(OH)2���ɡ�(4)����Ũ��ʱ����Ҫ�õ��ƾ��ơ�������������(5)���ˢܵ���Һ�к��д������Ȼ���������ѭ�����á�
�����Ѷȣ�һ��
2��ѡ���� ijKNO3��Һ�к�����KCl��K2SO4��Ca(NO3)2��������ȥ���ʣ��õ�������KNO3��Һ��������Լ�����ȷ˳���ǣ�
A��Ba(NO3)2��K2CO3��AgNO3��HNO3
B��K2CO3��Ba(NO3)2��AgNO3��HNO3
C��Ba(NO3)2��K2CO3��HNO3��AgNO3
D��AgNO3��Ba(NO3)2��K2CO3��HNO3
�ο��𰸣�D
����������Ȼ�������������ȥ������������ᱵ��ȥ���������̼��س�ȥ�����ڹ��������ᱵ����������Ҫ��̼���������������ȷ�Ĵ�ѡD��
�����Ѷȣ�һ��
3��ѡ���� ��Һ©���ǰ��ܶȲ�ͬ�һ������ܵ�Һ���������������и��������У����÷�Һ©�����з������
A�����Ȼ�̼��Һ��
B�����ͺͻ�����
C������ʳ��ˮ
D���ƾ���ˮ
�ο��𰸣�C
������������÷�Һ©������������Ϊ�������ܵ�Һ������
A����Һ�����������Ȼ�̼��B�������ͺͻ����ͻ��ܣ�C��ȷ������ʳ��ˮ�������ܣ�D�����ƾ���ˮ���ܣ�
�����Ѷȣ���
4��ʵ���� ��16�֣���ֻδ����ǩ���Լ�ƿ�зֱ�ʢװ��NaNO3��Һ��Na2CO3��Һ��Na2SO4��Һ��NaCl��Һ��ͨ������ʵ�齫������Һ�ֱ������밴ʵ�鲽��ش��������⡣
����֧�Թ��зֱ�ȡ������Һ��1mL���������ʵ�顣
��1������֧�Թ��зֱ����???????������????????�������??????�����ӷ�Ӧ����ʽ��????? ??????????????????????��
??????????????????????��
��2����ʣ����֧�Թ��зֱ����????????������?????????�������??????�����ӷ�Ӧ����ʽ��?????????????????????????????��
��3����ʣ����֧�Թ��зֱ����???? ????������????????�������???????�� ���ӷ�Ӧ����ʽ��?????????????????????????????????������ʵ���ж�û�������������????????????��
????������????????�������???????�� ���ӷ�Ӧ����ʽ��?????????????????????????????????������ʵ���ж�û�������������????????????��
�ο��𰸣���ÿ��1�֣����ӷ���ʽ2�֣��ޡ�������������1�֡���16�֣�
�����������
�����Ѷȣ�һ��
5��ѡ���� �������ʵ�����K2SO4��NaCl��Ba(NO3)2��AgNO3��Ͼ��Ⱥ����������У�����������ˮ�����裬���ã����ˡ�ȡ��Һ���ò��缫���һ��ʱ�䣬����������������������ͻ�ԭ�����������Ϊ
A.35.5�U108
B.108�U71
C.8�U1
D.1�U2
�ο��𰸣�C
�����������������������Һ�з�Ӧǡ������BaSO4��AgCl������ʣ�µ���Һ����൱�ڵ��ˮ�����������������ֱ������������������������Ϊ1:8��
�����Ѷȣ�����