微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知热化学方程式C2H2(g)+O2(g)=2CO2(g)+H2O(g);ΔH=-1256 kJ・mol-1,下列说法正确的是 ( )
A.乙炔的燃烧热为1256 kJ・mol-1
B.若转移10 mol电子,则消耗2.5 mol O2
C.若生成2 mol液态水,则ΔH=-2512 kJ・mol-1
D.若形成4 mol碳氧共用电子对,则放出的热量为2512 kJ
参考答案:B
本题解析:燃烧热是指1mol可燃物完全燃烧生成稳定的氧化物时所放出的能量。A不正确,氢对应的是液态水。1mol氧气得到4mol电子,所以选项B正确。△H和方程式的计量数及物质的状态有关系,C不正确。形成4 mol碳氧共用电子对,说明CO2是1mol,所以D是错误的。答案选B。
本题难度:一般
2、填空题 红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如图所示( 图中的△H表示生成1mol产物的数据)。根据图示,回答下列问题:

⑴P和Cl2反应生成PCl3(g)的热化学方程式 。
⑵PCl5(g)分解成PCl3(g)和Cl2的热化学方程式 。
⑶白磷能自燃,红磷不能自燃。白磷转变成红磷为 (“放”或“吸”) 热反应。如果用白磷替代红磷和Cl2反应生成1molPCl5的△H3,则△H3 △H1 (填“<”、“>” 或 “=”)。
参考答案:(1)P(s)+ 本题解析:
本题解析:
试题分析:(1)根据图示可知:P(s)+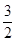 Cl2(g)=PCl3(g),反应物的总能量大于生成物的总能量,该反应是放热反应,反应热为△H=-306 kJ/mol,则热化学方程式为:P(s)+
Cl2(g)=PCl3(g),反应物的总能量大于生成物的总能量,该反应是放热反应,反应热为△H=-306 kJ/mol,则热化学方程式为:P(s)+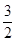 Cl2(g)=PCl3(g)△H="-306" kJ/mol。
Cl2(g)=PCl3(g)△H="-306" kJ/mol。
(2)根据图示可知:Cl2(g)+PCl3(g)=PCl5(g),中间产物的总能量大于最终产物的总能量,该反应是放热反应,△H=生成物总能量-反应物总能量=-93 kJ/mol;所以PCl5(g)=PCl3(g)+Cl2(g)是吸热反应;热化学方程式:PCl5(g)=PCl3(g)+Cl2(g)△H="+93" kJ/mol。
(3)白磷能自燃,红磷不能自燃,这说明白磷的总能量高于红磷的总能量,因此白磷转变成红磷为放热反应。由于白磷总能量高于红磷总能量,所以如果用白磷替代红磷和Cl2反应生成1molPCl5时放出的热量多,则反应热△H3<△H1。
考点:考查热化学方程式的书写、反应热的计算以及反应热的应用等
本题难度:一般
3、选择题 在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ,下列热化学方程式正确的是
A.CH3OH(l)+3/2O2(g)→CO2(g)+2H2O(l)△H="+725.8" kJ/mol
B.2CH3OH(l)+3O2(g)→2CO2(g)+4H2O(l)△H=-1452 kJ/mol
C.2CH3OH(l)+3O2(g)→2CO2(g)+4H2O(l)△H=-725.8 kJ/mol
D.2CH3OH(l)+3O2(g)→2CO2(g)+4H2O(l)△H="+1452" kJ/mol
参考答案:B
本题解析:A错,甲醇燃烧为放热反应;B正确;C错,反应热应为:△H=-1452 kJ/mol;D错,燃烧为放热反应;
本题难度:一般
4、选择题 下列反应前后物质的总能量变化可用下图表示的是
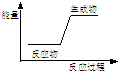
A.石灰石在高温下的分解反应
B.生石灰和水的反应
C.盐酸与氢氧化钠溶液的反应
D.木炭在氧气中燃烧
参考答案:A
本题解析:
试题分析:由能量变化图可知反应为吸热,而B、C、D项为放热反应。
考点:化学反应的能量变化。
本题难度:一般
5、选择题 一个燃烧天然气(主要成分是甲烷CH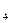 )的炉具,改成燃烧液化石油气(主要成分是C
)的炉具,改成燃烧液化石油气(主要成分是C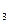 H
H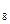 等)的炉具,其改造办法是(?)
等)的炉具,其改造办法是(?)
A.增大进空气的孔,适当减小燃气出孔
B.增大燃气出孔,适当减小进空气的孔
C.适当减小进空气的孔,同时减小燃气出孔
D.适当增大进空气的孔,并增大燃气出孔
参考答案:A
本题解析:CH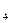 、C
、C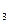 H
H 本题难度:一般
本题难度:一般